题目内容
元素M有多种氧化物,其中MO中含氧53.33%,那么化学式相对分子质量为76,含氧为63.16%的氧化物的化学式为
- A.MO
- B.M2O3
- C.MO2
- D.M2O5
B
分析:根据MO中含氧53.33%,计算出M的相对分子质量,然后计算出氧化物的化学式.
解答:根据MO中含氧53.33%,设M的相对原子质量为x,则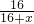 ×100%=53.33%,则x=14
×100%=53.33%,则x=14
A、由题干已知MO中含氧53.33%,故A不符合题意;
B、M2O3的相对分子质量=14×2+16×3=76,氧元素的质量分数=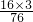 ×100%=63.16%,故符合题意;
×100%=63.16%,故符合题意;
C、MO2的相对分子质量=14+16×2=46,氧元素的质量分数=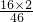 ×100%=69.57%,故不符合题意;
×100%=69.57%,故不符合题意;
D、M2O5的相对分子质量=14×2+16×5=108,氧元素的质量分数=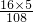 ×100%=74.07%,故不符合题意;
×100%=74.07%,故不符合题意;
故选B
点评:本题考查了化学式的有关计算,解答的关键是求出M的相对原子质量.
分析:根据MO中含氧53.33%,计算出M的相对分子质量,然后计算出氧化物的化学式.
解答:根据MO中含氧53.33%,设M的相对原子质量为x,则
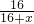 ×100%=53.33%,则x=14
×100%=53.33%,则x=14A、由题干已知MO中含氧53.33%,故A不符合题意;
B、M2O3的相对分子质量=14×2+16×3=76,氧元素的质量分数=
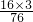 ×100%=63.16%,故符合题意;
×100%=63.16%,故符合题意;C、MO2的相对分子质量=14+16×2=46,氧元素的质量分数=
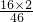 ×100%=69.57%,故不符合题意;
×100%=69.57%,故不符合题意;D、M2O5的相对分子质量=14×2+16×5=108,氧元素的质量分数=
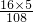 ×100%=74.07%,故不符合题意;
×100%=74.07%,故不符合题意;故选B
点评:本题考查了化学式的有关计算,解答的关键是求出M的相对原子质量.

练习册系列答案
相关题目