题目内容
1. X、Y、Z三种物质有如图所示的转化关系.
X、Y、Z三种物质有如图所示的转化关系.①若X为金属单质,Z为含X元素的可溶性盐.写出Y→Z且能体现酸的性质的反应方程式一个:CuO+H2SO4═CuSO4+H2O.
②若X为Ca(OH)2,则Y是CaCO3,Z是CaO.
分析 ①据金属和氧气反应生成金属氧化物,金属氧化物和酸反应生成可溶性的盐和水,据此分析解答;
②据氢氧化钙、碳酸钙和氧化钙的相互转化分析解答.
解答 解:
①据金属和氧气反应生成金属氧化物,金属氧化物和酸反应生成可溶性的盐和水,若X是铜,则Y是氧化铜,氧化铜和硫酸反应生成硫酸铜和水,其反应的化学方程式是:CuO+H2SO4═CuSO4+H2O;
②若X为Ca(OH)2,氢氧化钙可与二氧化碳、碳酸钠反应生成碳酸钙,碳酸钙高温生成氧化钙;
故答案为:
①CuO+H2SO4═CuSO4+H2O(合理答案均可);②CaCO3; CaO.
点评 明确物质之间的相互转化,物质的性质等知识,才能正确解答,较好考查了学生分析、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.氮气中氮元素的化合价为( )
| A. | -3 | B. | 0 | C. | +2 | D. | +5 |
4.影响碳的化学活动性的主要因素有( )
| A. | 空气 | B. | 温度 | C. | 日光 | D. | 水 |
9.下列各种物质中,颜色、状态都相同的是( )
| A. | 氧气和氮气 | B. | 铁和铜 | C. | 水和植物油 | D. | 酒精和食盐 |
6.正确读写化学符号是学好化学的基础,下列读法或写法正确的是( )
| A. | 3H--3个氢分子 | B. | 2H2O--2个水分子 | C. | 硫酸钾--KSO4 | D. | 氧化镁--Mg2O2 |
11.钢铁工业是国家工业的基础,工业上常用赤铁矿(主要成分氧化铁)冶炼铁,某化学兴趣小组模拟炼铁实验,实验过程中红色粉末全部变为黑色,并对试验过程中的现象进行探究.
【实验装置】
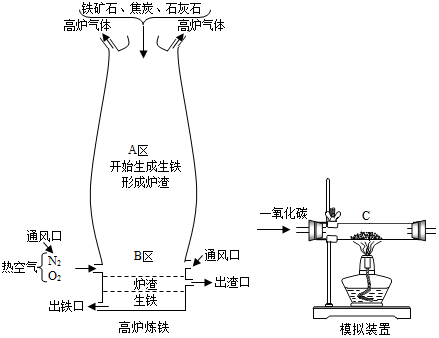
写出A区和B区所发生反应的主要方程式:
A区Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;B区C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2、CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
【提出问题】
观察黑色粉末有两种,黑色粉末成分是什么呢?
【查阅资料】
溶液中Fe2+和Fe3+同时存在是溶液呈黄色
【假设猜想】
猜想①:含有铁、氧化亚铁. 猜想②:含有铁、四氧化三铁. 猜想③:含有铁、氧化亚铁和四氧化三铁.
【实验方案】请写出实验操作,与表中结论相符的预期现象.
【交流反思】
(1)生铁口低于出渣口的原因生铁的密度大于炉渣的密度;
(2)在做模拟实验中发现其存在一个很不环保的缺陷,如何进缺陷:尾气没有处理;
处理尾气的方法:点燃尾气,或利用塑料袋收集尾气.
【实验装置】

写出A区和B区所发生反应的主要方程式:
A区Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;B区C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2、CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
【提出问题】
观察黑色粉末有两种,黑色粉末成分是什么呢?
【查阅资料】
| 物质 | 四氧化三铁 | 氧化亚铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 能 |
| 与盐酸反应溶液颜色 | 黄色 | 浅绿色 | 浅绿色 |
【假设猜想】
猜想①:含有铁、氧化亚铁. 猜想②:含有铁、四氧化三铁. 猜想③:含有铁、氧化亚铁和四氧化三铁.
【实验方案】请写出实验操作,与表中结论相符的预期现象.
| 实验方法 | 实验操作 | 预期现象 | 结论 |
| 物理方法 | 步骤1 | 黑色粉末全部被吸引 | 猜想②成立 |
| 化学方法 | 步骤2 | 产生气泡,溶液变成黄色 |
(1)生铁口低于出渣口的原因生铁的密度大于炉渣的密度;
(2)在做模拟实验中发现其存在一个很不环保的缺陷,如何进缺陷:尾气没有处理;
处理尾气的方法:点燃尾气,或利用塑料袋收集尾气.