题目内容
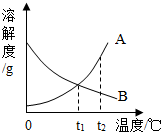 如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:(1)A、B两物质溶解度曲线相交点的意义:
(2)当B物质的溶液接近饱和时,采用三种方法均可使其变为饱和溶液.写出任意两种方法①
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法
专题:溶液、浊液与溶解度
分析:(1)由于在t1℃时,两物质的溶解度曲线交于一点,说明在该温度下,两物质的溶解度相等;
(2)B物质的溶解度随温度的升高而减小,B物质的不饱和溶液变为饱和溶液可采用升温的方法或加溶质.
(2)B物质的溶解度随温度的升高而减小,B物质的不饱和溶液变为饱和溶液可采用升温的方法或加溶质.
解答:解:
(1)由于在t1℃时,两物质的溶解度曲线交于一点,说明在该温度下,两物质的溶解度相等;
(2)增加溶质、蒸发溶剂都可使不饱和溶液变为饱和溶液,B物质的溶解度随温度的升高而减小,B物质的不饱和溶液变为饱和溶液还可采用升温的方法;故答案为:增加溶质、升高温度;
答案;
(1)在t1℃时,AB两物质的溶解度相同相同;
(2)
①加溶质;
②升高温度.
(1)由于在t1℃时,两物质的溶解度曲线交于一点,说明在该温度下,两物质的溶解度相等;
(2)增加溶质、蒸发溶剂都可使不饱和溶液变为饱和溶液,B物质的溶解度随温度的升高而减小,B物质的不饱和溶液变为饱和溶液还可采用升温的方法;故答案为:增加溶质、升高温度;
答案;
(1)在t1℃时,AB两物质的溶解度相同相同;
(2)
①加溶质;
②升高温度.
点评:本题难度不是很大,主要考查了固体溶解度的概念和固体溶解度曲线所表示的意义,从而培养学生对概念的理解能力和应用能力.

练习册系列答案
相关题目
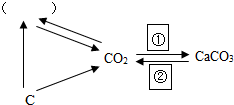 碳元素是构成物质种类最多的一种元素,许多物质都与我们的生活息息相关.
碳元素是构成物质种类最多的一种元素,许多物质都与我们的生活息息相关.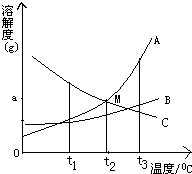 如图是A、B、C三种物质在水中的溶解度曲线,请回答:
如图是A、B、C三种物质在水中的溶解度曲线,请回答: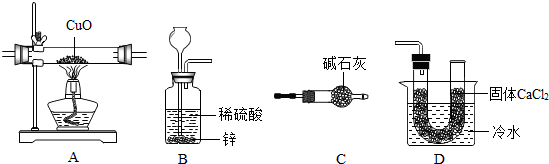
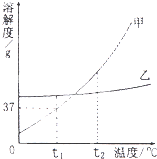 甲固体和乙固体的溶解度曲线如图所示:
甲固体和乙固体的溶解度曲线如图所示: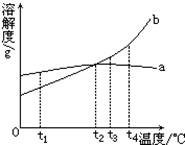 如图中曲线a.b是物质A.B的溶解度曲线.试根据图象回答:
如图中曲线a.b是物质A.B的溶解度曲线.试根据图象回答: