题目内容
18.如表实验方案中,不能达到实验目的是( )| 选项 | 实验目的 | 实验方案 |
| A | 分离铜粉和铁粉 | 用磁铁吸出 |
| B | 除去氯化钠固体中的少量碳酸钠 | 加入适量稀盐酸,充分反应后,蒸发 |
| C | 检验二氧化碳气体中含有少量一氧化碳 | 将混合气体依次通过灼热的氧化铁和澄清石灰水,观察澄清石灰水的变化 |
| D | 鉴别海水和蒸馏水 | 各取少量溶液于试管中,分别滴加硝酸钠溶液,观察试管中的溶液的变化 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、利用磁铁可以吸取铁粉的性质;
B、根据碳酸钠和盐酸反应产生氯化钠、水和二氧化碳,蒸发可以除去水蒸气分析;
C、根据实验设计中的目的是证明一氧化碳的存在,分析实验设计的科学性;
D、根据硝酸钠和氯化钠、水等都不反应分析.
解答 解:A、用磁铁除去铜粉中混有的少量铁粉,可以除去铁粉,故A方法正确;
B、碳酸钠和盐酸反应产生氯化钠、水和二氧化碳,再蒸发可以得到氯化钠固体,故B方法正确;
C、该方式是利用一氧化碳还原氧化铁生成二氧化碳的原理来验证一氧化碳的存在,所以实验开始时一定要先除掉混合物中的原有二氧化碳,以防止对实验的干扰,再检验一氧化碳的存在,故C方法错误;
D、硝酸钠和海水中的氯化钠、水都不反应,不能鉴别,故D方法错误;
故选项为:CD.
点评 本题难度不大,但综合性较强,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
9.下列叙述正确的是( )
| A. | 物质的水溶液一定是无色透明的 | |
| B. | 饱和溶液不一定比不饱和溶液浓 | |
| C. | 当饱和溶液的温度升高时,其溶质的溶解度一定变大 | |
| D. | 饱和溶液是纯净物,不饱和溶液是混合物 |
6.下列说法及化学符号都正确的是( )
| A. | 1个氯化钠分子:NaCl | B. | 2个氢元素:2H | ||
| C. | 硫酸铁:FeSO4 | D. | 保持氮气化学性质的最小微粒:N2 |
13.吴中区盛产茶叶,“碧螺春”享誉全国.绿茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,下列说法不正确的是( )
| A. | 单宁酸由碳、氢、氧三种元素组成 | |
| B. | 一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成 | |
| C. | 单宁酸分子中碳、氢、氧原子个数比为38:26:23 | |
| D. | 单宁酸中氧元素的质量分数最大 |
3.下列关于NaCl的说法正确的是( )
| A. | 生活中和工业上用的盐通常都为NaCl | |
| B. | 电解水时,为了增强溶液的导电性,可以加入NaCl | |
| C. | 我们获得NaCl的主要来源是用烧碱和盐酸反应制得 | |
| D. | 鉴别NaCl溶液和Na2CO3溶液可以用酚酞试剂 |
10.下列物质由离子构成的是( )
| A. | 水 | B. | 汞 | C. | 金刚石 | D. | 氯化钠 |
14.某兴趣小组发现了一包敞口放置的碱石灰样品,为探究其成分,同学们在实验室对这包碱石灰样品展开了探究.
【查阅资料】①碱石灰是由CaO和NaOH固体混合而成的,通常用于吸收二氧化碳和干燥气体.②CaCl2显中性.
【提出猜想】根据资料,小宏分析碱石灰样品的主要成分可能含有CaO、NaCl、NaOH、Na2CO3、Ca(OH)2、CaCO3.
他认为含有Na2CO3的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示),其他同学否定了NaCl的存在,原因是反应物中不含有氯元素,因此不能生成氯化钠.
【实验探究】小组讨论后设计如下实验进行,请补充探究过程.
【思考与分析】小涛同学经过分析认为步骤③的结论不准确,用化学方程式说明原因Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
【解释与结论】通过以上探究与分析:该碱石灰样品中一定含有Na2CO3、Ca(OH)2,步骤⑤所得溶液中除酚酞外还含有的溶质NaCl、BaCl2、NaOH.
【查阅资料】①碱石灰是由CaO和NaOH固体混合而成的,通常用于吸收二氧化碳和干燥气体.②CaCl2显中性.
【提出猜想】根据资料,小宏分析碱石灰样品的主要成分可能含有CaO、NaCl、NaOH、Na2CO3、Ca(OH)2、CaCO3.
他认为含有Na2CO3的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示),其他同学否定了NaCl的存在,原因是反应物中不含有氯元素,因此不能生成氯化钠.
【实验探究】小组讨论后设计如下实验进行,请补充探究过程.
| 实验步骤及操作 | 实验现象 | 结论 |
| ①取部分该样品于试管中,加少量水 | 无明显放热现象 | 碱石灰样品中不含CaO和NaOH |
| ②继续加足量水,振荡, ③过滤,向白色沉淀中滴加稀盐酸 | 产生白色沉淀 白色沉淀消失,并产生气泡 | 碱石灰样品中一定含有CaCO3 |
| ④从步骤②的试管中取少量上层清液于另一试管中, 向其中滴加过量BaCl2溶液 | 产生白色沉淀 |  |
| ⑤从步骤④的试管中取上层清液于另一试管中, 向其中滴加无色酚酞试液 | 溶液变红色 |
【解释与结论】通过以上探究与分析:该碱石灰样品中一定含有Na2CO3、Ca(OH)2,步骤⑤所得溶液中除酚酞外还含有的溶质NaCl、BaCl2、NaOH.
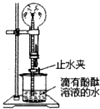 氨气在生产、生活中有广泛用途,研究其制取、性质和用途十分重要.
氨气在生产、生活中有广泛用途,研究其制取、性质和用途十分重要.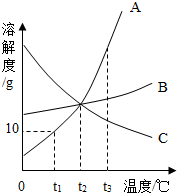 如图是A、B两种固体物质的溶解度曲线,请回答下列问题:
如图是A、B两种固体物质的溶解度曲线,请回答下列问题: