题目内容
某检测站对某品牌奶粉进行检测.取该奶粉样品100g,使其中蛋白质中的氮元素完全转变成氨气,用50g溶质质量分数为9.8%的稀硫酸恰好完全吸收生成硫酸铵.计算并回答下列问题:
(1)产生氨气的质量 g;
(2)该奶粉中含氮元素的质量分数 .
(1)产生氨气的质量
(2)该奶粉中含氮元素的质量分数
考点:根据化学反应方程式的计算,元素的质量分数计算
专题:有关化学方程式的计算
分析:(1)根据氨气与硫酸反应的方程式,由硫酸的质量求出氨气的质量;
(2)根据质量守恒定律,氨气中氮元素的质量,就是100g奶粉中氮元素的质量,最后求出该奶粉中含氮元素的质量分数.
(2)根据质量守恒定律,氨气中氮元素的质量,就是100g奶粉中氮元素的质量,最后求出该奶粉中含氮元素的质量分数.
解答:解:(1)设产生氨气的质量为x,
2NH3+H2SO4=(NH4)2SO4
34 98
x 50g×9.8%
=
解之得:x=1.7g.
(2)由质量守恒定律可知,该奶粉中含氮元素的质量分数为:
×=1.4%.
故答为:(1)1.7g (2)1.4%
2NH3+H2SO4=(NH4)2SO4
34 98
x 50g×9.8%
| 34 |
| 98 |
| x |
| 50g×9.8% |
(2)由质量守恒定律可知,该奶粉中含氮元素的质量分数为:
1.7g×
| ||
| 100g |
故答为:(1)1.7g (2)1.4%
点评:此题考查根据化学方程式的计算,此题解答较困难,综合性强,另外使学生明确一定质量的化合物中某元素的质量=化合物的质量×化合物中该元素的质量分数.

练习册系列答案
相关题目
煤、石油、天然气是重要的化石燃料,下列关于化石燃料的说法错误的是( )
| A、完全燃烧时都有二氧化碳生成 |
| B、石油是一种化工产品 |
| C、将煤隔绝空气加强热可制得焦炭 |
| D、煤、石油、天然气是不可再生能源 |
密闭容器中有甲、乙两种物质各10g,加热一段时间后测得容器中各物质的质量如下表所示
下列选项正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应后质量/g | 1.6 | X | 0.9 | 2.2 |
| A、该反应为化合反应 |
| B、X=5.3 |
| C、丙、丁一定是单质 |
| D、该反应中变化的甲和乙的质量比为84:53 |
反应H2+Cl2
2HCl中,反应前后没有改变的是( )
| ||
| A、分子的种类 |
| B、原子的种类 |
| C、元素的化合价 |
| D、物质的种类 |
宣传科学知识,反对伪科学是我们应尽的责任.下列说法具有科学道理的是( )
| A、干冰用于人工降雨 |
| B、用催化剂将水变成燃油 |
| C、人们可用肉眼看到硅原子 |
| D、中药是纯天然的,绝不含任何化学物质 |
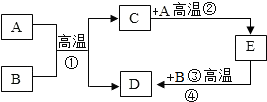
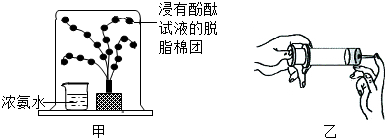 根据图中的相关信息回答下列问题.
根据图中的相关信息回答下列问题.