题目内容
6.为防止水体污染并回收某种金属,某工厂向含有硫酸铜的废水中加入一定量的铁粉,充分反应后过滤、洗涤、干燥得滤渣,取少量滤渣向其中加入稀盐酸产生气泡,则滤液中含有的物质是硫酸亚铁,写出向滤渣中加入稀盐酸发生反应的化学方程式Fe+2HCl=FeCl2+H2↑.分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢;位于前面的金属能把位于后面的金属从它们的化合物溶液中置换出来.
解答 解:因铁排在铜的前面,铁粉加入硫酸铜溶液中,铁可以置换出硫酸铜溶液中的铜,所以滤渣中一定含有生成的铜;又因为铁会置换出酸中的氢,而铜不会,滤渣中加入稀盐酸产生气泡,所以滤渣中一定含有过量的铁,综合分析可知滤渣中一定含有的物质是Fe和Cu,滤液中一定含有的溶质是:硫酸亚铁;产生气泡的反应是铁和盐酸的反应.
故答案为:硫酸亚铁; Fe+2HCl=FeCl2+H2↑.
点评 本题主要考查金属活动性顺序的应用,难度不大,需要注意两种金属与盐溶液反应时,活泼的金属先参与反应.

练习册系列答案
相关题目
16.关于“舌尖上的化学”,下列说法不科学的是( )
| A. | 为了健康,要均衡膳食 | |
| B. | 为使面包松软可口,制作时可添加适量碳酸氢钠 | |
| C. | 为预防大脖子病,可食用适量海带 | |
| D. | 为延长食品保质期,可添加大量防腐剂 |
14.下列物质中,含有氧分子的是( )
| A. | SO2 | B. | H2O2 | C. | O2 | D. | MnO2 |
11.下列各组物质按酸、碱、盐、氧化物顺序排列的是( )
| A. | H2SO4 Na2CO3 NaCl CO | B. | Mg(OH)2 CuSO4 HNO3 CO2 | ||
| C. | KOH HCl AgCl SO2 | D. | HNO3 NaOH CaCO3 H2O |
15.下列离子可在同一溶液中大量共存的是( )
| A. | SO42- NH4+ Na+ OH- | B. | H+ SO42- K+ CO32- | ||
| C. | Cl- K+ Ca2+ NO3- | D. | Ba2+ CO32- NO3- Na+ |
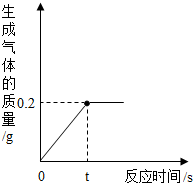 化学兴趣小组的同学取10g某锌样品(含少量杂质,且杂质不溶于水,也不与酸反应)于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7g时,恰好完全反应,生成气体的质量与反应时间的关系如右图所示,试回答下列问题:
化学兴趣小组的同学取10g某锌样品(含少量杂质,且杂质不溶于水,也不与酸反应)于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7g时,恰好完全反应,生成气体的质量与反应时间的关系如右图所示,试回答下列问题: