题目内容
17.化学是研究物质的组成、结构、性质及其变化规律的自然科学.(1)从图中能获取的信息是ACD.
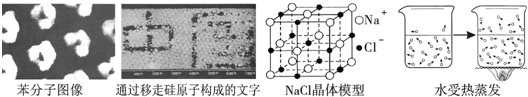
A.分子之间有间隔 B.硅原子是由原子核和电子构成
C.水分子受热运动速率加快 D.构成物质的粒子有分子、原子和离子
(2)兴趣小组同学利用以下实验探究氨气的性质,下图从左到右依次是实验步骤及相应的现象.
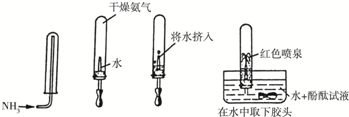
根据上图信息,能得出的结论有氨气密度比空气小、氨气易溶于水、氨水显碱性.
解析:
①第一幅图:氨气可以用向下排空气法收集,说明氨气的密度比空气小.
②第二、三、四幅图:胶头滴管中的水挤入试管后,试管内的气压减小,说明氨气极易溶于水,且形成的氨水可以使无色酚酞试液变成红色.所以氨气不能(填“能”或者“不能”)用排水法收集.
(3)在点燃条件下,A和B反应生成C和D.反应前后分子变化的微观示意图如下所示.
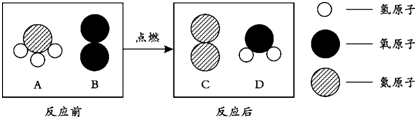
①该反应的基本反应类型为置换反应.
②该反应中A、C两种物质的质量比为17:14.
解析:
①先写出该反应中四种物质的化学式:A:NH3 B:O2 C:N2 D:H2O.
②写出该反应的化学方程式:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
③根据化学方程式,写出相关物质的相对分子质量、已知量、未知量,进行计算:17:14.
分析 (1)根据图片分析微粒的性质以及构成物质微粒的种类;(2)氨气是一种密度比空气小、易溶于水的气体,其水溶液呈碱性.本题就是以图示的形式让同学们归纳氨气的性质,可以考虑氨气以上具有的性质;(3)①单质和化合物反应生成单质和化合物属于置换反应,②写出化学方程式配平后计算相对分子质量比解析:①根据图示写出化学式即可;②根据化学方程式的写法写出化学方程式;③根据化学方程式的计算方法回答.
解答 解:(1)A、由苯分子图象及水受热蒸发的图片,都可以表示出构成物质的分子间存在间隔;故A正确;
B、通过移走硅原子构成文字的图片中的文字是移走原子后所形成的,此图表示由原子构成的物质中原子可以进行移动但却不能说明原子的内部构成;故B不正确;
C、水受热蒸发前后相比,加热后扩散入空气中的水分子明显增加,可说明受热能使水分子运动速率加快,故C正确;
D、从四幅图片可以看出苯和水由分子构成,氯化钠由离子构成,硅由原子构成,所以构成物质的微粒有:分子、原子、离子.故D正确
(2)根据图示信息可以看出,用的是向下排空气法收集一试管氨气,可知氨气具有密度比空气小的性质,把水挤入试管后会形成喷泉,说明试管内压强减小,而压强减小的原因就是氨气溶解在水中,可知氨气具有易溶于水的性质;能形成红色喷泉,说明氨水能使酚酞试液变红,说明氨水显碱性.故答为:氨气密度比空气小;氨气易溶于水;氨水显碱性;①向下排空气;比空气小;②减小;溶于;红;不能;
(3)①由图示可知反应物是一种单质和一种化合物,生成物是一种单质和一种化合物,属于置换反应;②由图示可知:A是NH3;B是O2;C是N2;D是H2O,所以化学方程式是:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O 所以A与C的质量比是:68:56=17:14.
68 56
故答案为:(1)ACD;(2)氨气密度比空气小;氨气易溶于水;氨水显碱性;①向下排空气;比空气小;②减小;溶于;红;不能;
(3)①置换反应;②17:14;解析:①NH3;O2;N2;H2O ②4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;③17:14.
点评 构成物质的微粒有分子、原子和离子三种;氯化钠等物质由离子构成,金属单质、稀有气体等物质由原子直接构成,其它物质则由分子构成,正确的分子图片信息结合微粒的性质是解题的关键;氨气是一种重要的气体,本题用图示的形式考查了氨气的性质,可以依据已有知识做出回答.

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案 燃烧是人类最早利用的化学反应之一,但是燃烧引发的火灾也会给人类带来灾难.已知某化合物的着火点为t1,该物质易在空气中失火,则如图所示的A、B、C、D点中,表示完全可以灭火的是( )
燃烧是人类最早利用的化学反应之一,但是燃烧引发的火灾也会给人类带来灾难.已知某化合物的着火点为t1,该物质易在空气中失火,则如图所示的A、B、C、D点中,表示完全可以灭火的是( )| A. | A点和D点 | B. | A点和B点 | C. | B点和C点 | D. | C点和D点 |
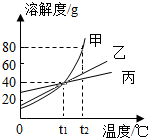 如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息正确的是( )| A. | 甲、乙、丙三者的溶解度相同 | |
| B. | t1℃时100g甲的饱和溶液中含有40g甲 | |
| C. | t2℃时,往100 g水中加入90 g甲,充分搅拌后得到190 g甲的溶液 | |
| D. | t1℃时甲、乙、丙三者饱和溶液的溶质质量分数相等 |
 2013年浙大实验室诞生了世界最轻的材料-“碳海绵”,其密度仅是空气的$\frac{1}{6}$,这种材料放桃花花蕊上,花蕊也能承受重压(如图).“碳海绵”具备高弹性和强吸附性,主要成分是石墨烯和碳纳米管(两者都是碳单质).下列关于“碳海绵”的说法错误的是( )
2013年浙大实验室诞生了世界最轻的材料-“碳海绵”,其密度仅是空气的$\frac{1}{6}$,这种材料放桃花花蕊上,花蕊也能承受重压(如图).“碳海绵”具备高弹性和强吸附性,主要成分是石墨烯和碳纳米管(两者都是碳单质).下列关于“碳海绵”的说法错误的是( )| A. | “碳海绵”完全燃烧的产物是二氧化碳 | |
| B. | “碳海绵”的高弹性和强吸附性,属于物理性质 | |
| C. | “碳海绵”可能具有疏松多孔的结构 | |
| D. | “碳海绵”是纯净物 |
| A. | O2 | B. | N2 | C. | CO2 | D. | 稀有气体 |


