题目内容
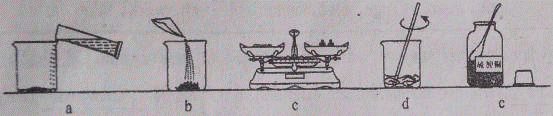
某补钙药剂的标签主要内容如图所示,现测定该钙片钙含量是否符合标注,做以下实验:取10片该钙片,放人干燥、洁净的烧杯中,再向烧杯中加人50g某浓度盐酸,恰好完全反应(钙片中其它成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出).反应后称量烧杯内剩余物质的质量为64. 5g.
(1)反应中生成____________g二氧化碳,此反反应的基本反应类型为_________;
(2)通过计算说明实际钙含量是否与标注相符;
(3)试计算所用稀盐酸的溶质质量分数.

【答案】(1)5.5;复分解反应;(2)不符合;(3)18.25%
【解析】(1)根据质量守恒定律可知,生成二氧化碳的质量为:10×2g+50g-64.5g=5.5g
(2)解:设10片钙片中碳酸钙的质量为x,50g盐酸中氯化氢的质量为y、
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
100 73 44
X y 5.5g
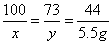
X=12.5g y=9.125g
则每片钙片中含钙: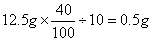
0.5g<0.6g,所以不符合
稀盐酸中溶质的质量分数为: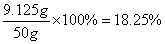

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
欲测定某锌-铜合金中铜的质量分数,进行如下实验:取合金样品10g放入烧杯中,将60g稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量/g | 20 | 20 | 20 |
| 生成气体质量/g | 0.08 | m | 0.04 |
请回答下列问题并计算:
(1)第二次实验时生成气体质量m= g;
(2)计算该合金样品中铜的质量分数。
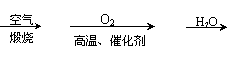 硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。
硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。 沾到皮肤上的处理方法是 。
沾到皮肤上的处理方法是 。