题目内容
甲、乙、丙三位同学分别取某石灰石样品与50g盐酸进行实验,所得结果如下:| 实 验 | 甲 | 乙 | 丙 |
| 加入样品的质量∕g | 5 | 10 | 15 |
| 生成CO2的质量∕g | 1.76 | 3.52 | 4.40 |
(2)盐酸中溶质的质量分数是______.
【答案】分析:(1)由表中数据知甲、乙中碳酸钙完全反应,因此可据甲、乙两组数据根据化学方程式来计算石灰石中碳酸钙的质量分数.
(2)由表中数据知丙中盐酸完全反应,因此可据丙中二氧化碳的质量根据化学方程式计算盐酸的溶质质量分数.
解答:解:(1)设石灰石样品中碳酸钙的质量分数为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
5g×x 1.76g
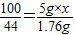
x=80.0%
答:该石灰石样品中碳酸钙的质量分数是80.0%.
(2)设盐酸中溶质的质量分数为y,
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
50g×y 4.4g
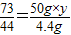
y=14.6%
答:盐酸中溶质的质量分数是14.6%.
点评:本题考查含杂质物质的化学方程式计算和溶质质量分数的计算,难度较大.
(2)由表中数据知丙中盐酸完全反应,因此可据丙中二氧化碳的质量根据化学方程式计算盐酸的溶质质量分数.
解答:解:(1)设石灰石样品中碳酸钙的质量分数为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
5g×x 1.76g
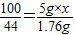
x=80.0%
答:该石灰石样品中碳酸钙的质量分数是80.0%.
(2)设盐酸中溶质的质量分数为y,
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
50g×y 4.4g
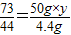
y=14.6%
答:盐酸中溶质的质量分数是14.6%.
点评:本题考查含杂质物质的化学方程式计算和溶质质量分数的计算,难度较大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目