题目内容
17.下列反应符合事实的是( )| A. | BaCO3+H2SO4=BaSO4↓+H2O+CO2↑ | B. | Fe+3AgNO3=Fe(NO3)3+3Ag | ||
| C. | N2+2O2$\frac{\underline{\;点燃\;}}{\;}$ 2NO2 | D. | Na2CO3+2KNO3=2NaNO3+K2CO3 |
分析 根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
解答 解:A、该化学方程式书写完全正确.
B、铁与硝酸银溶液反应生成硝酸亚铁溶液和银,正确的化学方程式应为Fe+2AgNO3=Fe(NO3)2+2Ag.
C、氮气与氧气在点燃条件下不反应,故选项错误.
D、碳酸钠与硝酸钾交换成分没有沉淀、气体或水生成,不能发生复分解反应,故选项错误.
故选:A.
点评 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.

练习册系列答案
相关题目
7.现将X、Y两种金属片分别插入硫酸铜溶液中,Y无明显变化,X表面有铜析出,则X、Y、Cu三种金属的活动性由强到弱的顺序是( )
| A. | X>Cu>Y | B. | Cu>X>Y | C. | Y>Cu>X | D. | X>Y>Cu |
2.科学探究是奇妙的过程,请你一起参与实验探究,并填写下列空白.
【提出问题】小森同学在滴加FeCl3溶液时,不小心把滴加FeCl3溶液的滴管放入到盛“双氧水”(过氧化氢)的试剂瓶中,发现有大量的气泡产生,小森联想到用二氧化锰可作过氧化氢分解的催化剂,他想FeCl3溶液能否也可以作过氧化氢分解的催化剂呢?
于是他做了以下探究:
【猜想与假设】FeCl3溶液能作过氧化氢分解的催化剂.
【设计与实验】请你完成下表:
【讨论与反思】已知FeCl3溶液含有H2O、Fe3+和Cl-三种微粒,小森又做了三种猜想:
猜想1:真正催化分解H2O2的是FeCl3溶液中的H2O;
猜想2:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
猜想3:真正催化分解H2O2的是FeCl3溶液中的Cl-
你认为最不可能的是猜想猜想1,理由是过氧化氢溶液中有水.
小森同学又对余下的两种猜想进行了实验探究.
(1)向盛有5mL 15%的H2O2溶液的试管中加入少量的HCl,然后把带火星的木条伸入试管中,无明显现象,则猜想3不成立;
(2)向盛有5mL 15%的H2O2溶液的试管中加入少量的硫酸铁溶液,然后把带火星的木条伸入试管中,观察到试管中有大量气泡产生,带火星的木条复燃,则猜想2成立.
【提出问题】小森同学在滴加FeCl3溶液时,不小心把滴加FeCl3溶液的滴管放入到盛“双氧水”(过氧化氢)的试剂瓶中,发现有大量的气泡产生,小森联想到用二氧化锰可作过氧化氢分解的催化剂,他想FeCl3溶液能否也可以作过氧化氢分解的催化剂呢?
于是他做了以下探究:
【猜想与假设】FeCl3溶液能作过氧化氢分解的催化剂.
【设计与实验】请你完成下表:
| 实验步骤 | 实验现象 | 解释与结论 |
| 在一支试管中加入5mL 15%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管 | 有气泡冒出,木条复燃 | FeCl3溶液可以催化分解H2O2 |
猜想1:真正催化分解H2O2的是FeCl3溶液中的H2O;
猜想2:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
猜想3:真正催化分解H2O2的是FeCl3溶液中的Cl-
你认为最不可能的是猜想猜想1,理由是过氧化氢溶液中有水.
小森同学又对余下的两种猜想进行了实验探究.
(1)向盛有5mL 15%的H2O2溶液的试管中加入少量的HCl,然后把带火星的木条伸入试管中,无明显现象,则猜想3不成立;
(2)向盛有5mL 15%的H2O2溶液的试管中加入少量的硫酸铁溶液,然后把带火星的木条伸入试管中,观察到试管中有大量气泡产生,带火星的木条复燃,则猜想2成立.
9.材料是时代进步的重要标志,材料为人类作出了巨大的贡献.下列物品所使用的主要材料属于有机合成材料的是( )
| A. |  聂耳铜像 | B. |  塑料桶 | C. |  纯棉T恤 | D. |  陶瓷制品 |
6.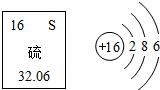 硫磺是我国四大发明之一火药的成分之一.如图是元素周期表中硫元素的相关信息及其原子结构示意图,下列说法正确的是( )
硫磺是我国四大发明之一火药的成分之一.如图是元素周期表中硫元素的相关信息及其原子结构示意图,下列说法正确的是( )
 硫磺是我国四大发明之一火药的成分之一.如图是元素周期表中硫元素的相关信息及其原子结构示意图,下列说法正确的是( )
硫磺是我国四大发明之一火药的成分之一.如图是元素周期表中硫元素的相关信息及其原子结构示意图,下列说法正确的是( )| A. | 硫元素属于金属元素 | B. | 硫原子核外有16个电子 | ||
| C. | 硫的相对原子质量为32.06g | D. | 硫原子在化学反应中容易失去电子 |