题目内容
2013年央视3?15晚会曝光:某地区某些企业违反国家卫生规定,用回收的垃圾废纸,生产过程中经烧碱和荧光增白剂处理,生产劣质不卫生餐巾纸.根据所学知识回答下列问题:
(1)“烧碱”是氢氧化钠的俗称,它通常又被称为 ;
(2)采访中工人说它“烧劲大”指的是它 性强;中学实验室中要称取一定质量的氢氧化钠用烧杯而不用纸称量的原因是 .
(3)氢氧化钠固体有很强的吸水性,与生石灰按比例混合后称为碱石灰,是常用的气体干燥剂,根据你学过的知识,写出生石灰吸水后反应的化学方程式: ;下列气体不能用碱石灰干燥的是 (填序号)①CO2 ②CO ③H2 ④O2 ⑤SO2
(4)兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验.请你与他们一起完成以下探究活动:
【对固体猜想】
猜想Ⅰ:全部是NaOH; 猜想Ⅱ:全部是Na2CO3; 猜想Ⅲ:是NaOH和Na2CO3混合物.
【实验设计】
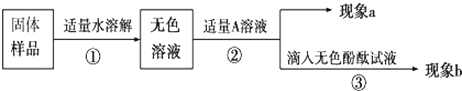
【现象及结论】
①若现象a为有气泡产生,则加入的A溶液是 ,说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是
②若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为 (填化学式),该实验 (填“能”或“不能”)说明样品中有NaOH.
③若A是CaCl2溶液,当实验现象a为 ,并且现象b为 ,则猜想Ⅱ成立.
【反思】久置的氢氧化钠变质的原因是(用化学方程式表示) .
(1)“烧碱”是氢氧化钠的俗称,它通常又被称为
(2)采访中工人说它“烧劲大”指的是它
(3)氢氧化钠固体有很强的吸水性,与生石灰按比例混合后称为碱石灰,是常用的气体干燥剂,根据你学过的知识,写出生石灰吸水后反应的化学方程式:
(4)兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验.请你与他们一起完成以下探究活动:
【对固体猜想】
猜想Ⅰ:全部是NaOH; 猜想Ⅱ:全部是Na2CO3; 猜想Ⅲ:是NaOH和Na2CO3混合物.
【实验设计】

【现象及结论】
①若现象a为有气泡产生,则加入的A溶液是
②若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为
③若A是CaCl2溶液,当实验现象a为
【反思】久置的氢氧化钠变质的原因是(用化学方程式表示)
考点:实验探究物质的组成成分以及含量,生石灰的性质与用途,常见碱的特性和用途,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据氢氧化钠的俗称进行分析;
(2)根据氢氧化钠具有强烈的腐蚀性进行分析;
(3)根据生石灰吸水后反应氢氧化钙以及碱石灰属于碱性干燥剂进行分析;
(4)①根据氢氧化钠能与二氧化碳发生反应生成水和碳酸钠,氢氧化钠吸收空气中的水分及二氧化碳而变质进行分析;
②根据氢氧化钠变质后的产物为碳酸钠,而碳酸钠溶液也呈碱性,可以使酚酞变红,所以不能用酚酞试液检验Na0H是否变质进行分析;
③根据氢氧化钠的性质进行分析,氢氧化钠露置在空气中易与二氧化碳反应生成碳酸钠而变质,反应的程度不同,则变质的程度不同;检验碳酸盐使用的是加酸化气的方法或加入含有可溶性钙离子、钡离子的方法,要证明含有氢氧化钠,则需要除去碳酸钠再进行检验,且加入的试剂与碳酸钠反应后不能生成显碱性的物质进行分析;
[反思]根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析.
(2)根据氢氧化钠具有强烈的腐蚀性进行分析;
(3)根据生石灰吸水后反应氢氧化钙以及碱石灰属于碱性干燥剂进行分析;
(4)①根据氢氧化钠能与二氧化碳发生反应生成水和碳酸钠,氢氧化钠吸收空气中的水分及二氧化碳而变质进行分析;
②根据氢氧化钠变质后的产物为碳酸钠,而碳酸钠溶液也呈碱性,可以使酚酞变红,所以不能用酚酞试液检验Na0H是否变质进行分析;
③根据氢氧化钠的性质进行分析,氢氧化钠露置在空气中易与二氧化碳反应生成碳酸钠而变质,反应的程度不同,则变质的程度不同;检验碳酸盐使用的是加酸化气的方法或加入含有可溶性钙离子、钡离子的方法,要证明含有氢氧化钠,则需要除去碳酸钠再进行检验,且加入的试剂与碳酸钠反应后不能生成显碱性的物质进行分析;
[反思]根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析.
解答:解:(1)氢氧化钠的俗称是:烧碱、火碱、苛性钠;
(2)采访中工人说它“烧劲大”指的是它腐蚀性强,氢氧化钠具有强烈的腐蚀性和吸水性,中学实验室中要称取一定质量的氢氧化钠,应放在用表面皿盖住的小烧杯中和天平左盘;
(3)生石灰吸水后反应氢氧化钙,反应的化学方程式是:CaO+H2O═Ca(OH)2;碱石灰属于碱性干燥剂,不能干燥酸性气体,所以不能干燥二氧化碳和二氧化硫,故选:①⑤;
(4)①氢氧化钠变质生成的是碳酸钠,如果加入A后产生气泡,则加入的物质是酸,可以是稀盐酸,盐酸能与碳酸钠反应生成氯化钠、水和二氧化碳,该反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
②氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以白色沉淀是碳酸钙,其化学式为:CaCO3;生成的氢氧化钠能使酚酞试液变红,所以不能确定原固体中是否含有氢氧化钠;
③若全部是碳酸钠,则加入的氯化钙能与碳酸钠反应生成碳酸钙白色沉淀和氯化钠,生成的氯化钠的水溶液呈中性,不能使酚酞试液变红,所以现象a为产生白色沉淀,现象b为酚酞不变色;
[反思]:氢氧化钠吸收空气中的水潮解后和空气中的二氧化碳生成碳酸钠和水,因此,与空气接触的氢氧化钠溶液会变质,该反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
故答案为:
(1)火碱;
(2)腐蚀,氢氧化钠有吸水性和腐蚀性;
(3)CaO+H2O═Ca(OH)2,①⑤;
(4)①稀盐酸,Na2CO3+2HCl═2NaCl+H2O+CO2↑;
②CaCO3,不能;
③有白色沉淀生成,无色酚酞试液不变色;
[反思]:2NaOH+CO2═Na2CO3+H2O.
(2)采访中工人说它“烧劲大”指的是它腐蚀性强,氢氧化钠具有强烈的腐蚀性和吸水性,中学实验室中要称取一定质量的氢氧化钠,应放在用表面皿盖住的小烧杯中和天平左盘;
(3)生石灰吸水后反应氢氧化钙,反应的化学方程式是:CaO+H2O═Ca(OH)2;碱石灰属于碱性干燥剂,不能干燥酸性气体,所以不能干燥二氧化碳和二氧化硫,故选:①⑤;
(4)①氢氧化钠变质生成的是碳酸钠,如果加入A后产生气泡,则加入的物质是酸,可以是稀盐酸,盐酸能与碳酸钠反应生成氯化钠、水和二氧化碳,该反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
②氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以白色沉淀是碳酸钙,其化学式为:CaCO3;生成的氢氧化钠能使酚酞试液变红,所以不能确定原固体中是否含有氢氧化钠;
③若全部是碳酸钠,则加入的氯化钙能与碳酸钠反应生成碳酸钙白色沉淀和氯化钠,生成的氯化钠的水溶液呈中性,不能使酚酞试液变红,所以现象a为产生白色沉淀,现象b为酚酞不变色;
[反思]:氢氧化钠吸收空气中的水潮解后和空气中的二氧化碳生成碳酸钠和水,因此,与空气接触的氢氧化钠溶液会变质,该反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
故答案为:
(1)火碱;
(2)腐蚀,氢氧化钠有吸水性和腐蚀性;
(3)CaO+H2O═Ca(OH)2,①⑤;
(4)①稀盐酸,Na2CO3+2HCl═2NaCl+H2O+CO2↑;
②CaCO3,不能;
③有白色沉淀生成,无色酚酞试液不变色;
[反思]:2NaOH+CO2═Na2CO3+H2O.
点评:本题主要考查了学生运用化学知识分析解决生活当中具体问题的能力,本类试题涉及的知识点比较分散,在课本上也比较分散,所以平时学习要经常进行整理.

练习册系列答案
相关题目
NO是一种大气污染物,它是一种无色气体,难溶于水,密度比空气略大,在空气中能与氧气迅速反应而生成红棕色的NO2气体.在实验室中,收集的方法是( )
| A、排水集气法 |
| B、向上排空气集气法 |
| C、向下排空气集气法 |
| D、排水集气法或向上排空气集气法 |
氧化物与X的关系可用如图表示,则X不可能是( )

| A、混合物 | B、纯净物 |
| C、化合物 | D、含氧化合物 |
下列化学用语表达正确的是( )
A、钠原子结构示意图: |
| B、两个钠离子:2Na+ |
| C、两个氮分子:2N |
| D、五氧化二氮:N5O2 |
物质的用途和性质密切相关.下列用途主要是利用其化学性质的是( )
| A、干冰做制冷剂 |
| B、金刚石作装饰品 |
| C、氢气作高能燃料 |
| D、铜丝作导线 |
下列广告用语从化学角度看,表述科学的是( )
| A、“K”牌咖啡,滴滴香浓,决不含任何化学物质 |
| B、“雪山牌”矿泉水,真正的纯水 |
| C、“大自然”牌蔬菜,天然种植,不含任何元素,真正的“绿色”食品 |
| D、食用合格“碘盐”,可预防某种甲状腺疾病 |
 小熠同学为补充维生素,服用XX牌多维元素片,该药品标签如图所示.请你计算:
小熠同学为补充维生素,服用XX牌多维元素片,该药品标签如图所示.请你计算: