题目内容
17.实验室常用氢氧化钠溶液来吸收一种有毒气体-氯气,其反应原理为:Cl2+2NaOH═X+NaClO+H2O,则X的化学式为NaCl,将氯气通入石灰水中也会发生类似反应,则反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物R的化学式.氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,写出反应的化学方程式即可.
解答 解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式Cl2+2NaOH═X+NaClO+H2O,反应前钠、氧、氢、氯原子个数分别为2、2、2、2,反应后的生成物中钠、氧、氢、氯原子个数分别为1、2、2、1,根据反应前后原子种类、数目不变,则每个X分子由1个钠原子和1个氯原子构成,则物质R的化学式为为NaCl.
氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,反应的化学方程式为:2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O.
故答案为:NaCl;2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
点评 本题难度不大,利用化学反应前后原子守恒来确定物质的化学式以及化学式的写法等是正确解答此类题的关键.

练习册系列答案
相关题目
6.分类法是学习化学的重要思想方法.现有下列三组物质:
A、空气、熟石灰、冰水、蔗糖
B.KOH、C2H5OH、Ca(OH)2、NH3•H2O
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白:
(2)请仿照检验CO2的反应原理,写出SO2与NaOH溶液反应的化学反应方程式SO2+2NaOH=Na2SO3+H2O.
A、空气、熟石灰、冰水、蔗糖
B.KOH、C2H5OH、Ca(OH)2、NH3•H2O
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白:
| 组别 | A组 | B组 | C组 |
| 分类标准 | 纯净物 | 碱 | ①盐 |
| 不属于上述分类标准的物质 | 空气 | ②C2H5OH | SO2 |
20.为了研究物质的溶解现象,设计并进行了如下实验,下列说法不正确的是( )
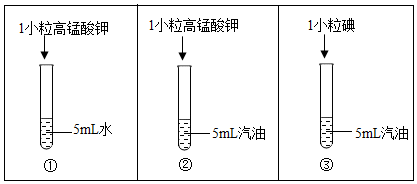

| A. | 实验①中的固体溶解,形成紫红色溶液;实验②中的固体几乎不溶解 | |
| B. | 设计实验②、③的目的是比较高锰酸钾和碘在汽油中溶解情况 | |
| C. | 对比实验①、②可得出的结论是高锰酸钾在水中的溶解性比汽油中的好 | |
| D. | 实验说明不同物质在同一溶剂中溶解性是相同的,同一种物质在不同溶剂中溶解性也是相同的 |
 A、B、C三种物质的溶解度曲线如图所示.据图回答:
A、B、C三种物质的溶解度曲线如图所示.据图回答: 人类在生产和生活中广泛使用金属.请回答:
人类在生产和生活中广泛使用金属.请回答: