题目内容
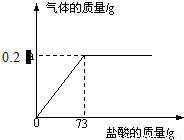
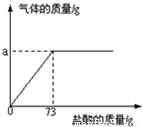
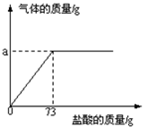 商家为谋取更大利益,用假黄金制作首饰蒙骗消费者.假黄金和黄金的颜色相似,用肉眼很难区分,一般采用加入稀盐酸判别黄金的真假.某校化学学习小组为了测定假黄金(铜-锌合金)中铜的质量分数,取10.0g假黄金与溶质的质量分数为10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图.
商家为谋取更大利益,用假黄金制作首饰蒙骗消费者.假黄金和黄金的颜色相似,用肉眼很难区分,一般采用加入稀盐酸判别黄金的真假.某校化学学习小组为了测定假黄金(铜-锌合金)中铜的质量分数,取10.0g假黄金与溶质的质量分数为10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图.(1)a=
0.2
0.2
.(2)假黄金中铜的质量分数?
(3)10.0g假黄金与溶质的质量分数为10%的盐酸恰好完全反应时所得不饱和溶液中溶质的质量分数为多少?(保留一位小数)
分析:由金属活动性顺序表可知假黄金中铜不能与盐酸反应,而锌能与盐酸反应;
(1)从图示可得盐酸的质量,利用盐酸的溶质质量分数可知其反应的氯化氢质量,然后依据氯化氢的质量可求生成氢气的质量;
(2)根据锌与盐酸反应的化学方程式,已知所用盐酸的质量和质量分数,能够计算出铜锌合金中的质量分数.
(3)所得溶液质量应该是物质的总质量减去不溶性杂质和生成的气体的质量,据此对生成的溶液溶质质量分数进行计算即可;
(1)从图示可得盐酸的质量,利用盐酸的溶质质量分数可知其反应的氯化氢质量,然后依据氯化氢的质量可求生成氢气的质量;
(2)根据锌与盐酸反应的化学方程式,已知所用盐酸的质量和质量分数,能够计算出铜锌合金中的质量分数.
(3)所得溶液质量应该是物质的总质量减去不溶性杂质和生成的气体的质量,据此对生成的溶液溶质质量分数进行计算即可;
解答:解:设锌的质量为x,生成氯化锌的质量为y,生成氢气的质量为z.
Zn+2HCl=ZnCl2+H2↑
65 73 136 2
x 73g×10% y z
=
=
=
x=6.5g
y=13.6g
z=0.2g
(1)由以上计算知a的值为0.2;
(2)假黄金中铜的质量分数为:
×100%=35%;
(3)所得不饱和溶液中溶质的质量分数为:
×100%=17.2%
故答案为:(1)0.2;
答:(2)假黄金中铜的质量分数为35%;
(3)所得不饱和溶液中溶质的质量分数为17.2%;
Zn+2HCl=ZnCl2+H2↑
65 73 136 2
x 73g×10% y z
| 65 |
| x |
| 73 |
| 73g×10% |
| 136 |
| y |
| 2 |
| z |
x=6.5g
y=13.6g
z=0.2g
(1)由以上计算知a的值为0.2;
(2)假黄金中铜的质量分数为:
| 10g-6.5g |
| 10g |
(3)所得不饱和溶液中溶质的质量分数为:
| 13.6g |
| 6.5g+73g-0.2g |
故答案为:(1)0.2;
答:(2)假黄金中铜的质量分数为35%;
(3)所得不饱和溶液中溶质的质量分数为17.2%;
点评:本题主要考查有关化学方程式的计算和质量分数的计算,难度不大.从图象中得到“当加入73g稀盐酸时,合金中的锌恰好反应完全,产生ag氢气”的信息是解题的关键.

练习册系列答案
相关题目
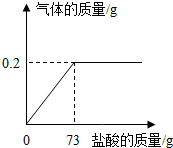 (2013?普宁市模拟)商家为谋取更大利益,用假黄金制作首饰蒙骗消费者.假黄金和黄金的颜色相似.某校化学学习小组为了测定假黄金(铜-锌合金)中铜的质量分数,取10.0g假黄金与溶质的质量分数为10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图.
(2013?普宁市模拟)商家为谋取更大利益,用假黄金制作首饰蒙骗消费者.假黄金和黄金的颜色相似.某校化学学习小组为了测定假黄金(铜-锌合金)中铜的质量分数,取10.0g假黄金与溶质的质量分数为10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图. (2012?普宁市一模)商家为谋取更大利益,用假黄金制作首饰蒙骗消费者.假黄金和黄金的颜色相似,用肉眼很难区分,一般采用加入稀盐酸判别黄金的真假.某校化学学习小组为了测定假黄金(铜-锌合金)中铜的质量分数,取10.0g假黄金与溶质的质量分数为10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图.
(2012?普宁市一模)商家为谋取更大利益,用假黄金制作首饰蒙骗消费者.假黄金和黄金的颜色相似,用肉眼很难区分,一般采用加入稀盐酸判别黄金的真假.某校化学学习小组为了测定假黄金(铜-锌合金)中铜的质量分数,取10.0g假黄金与溶质的质量分数为10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图.