题目内容
20.(1)在宏观、微观和符号之间建立联系是化学学科的特点.下列是氟元素、钠元素、氯元素在元素周期表中的信息和相应四种粒子的结构示意图.请回答下列问题:

氯元素的相对原子质量为22.99;由氟元素和钠元素形成的化合物的化学式为NaF;D元素应处于元素周期表中的第3周期.
(2)氯气是一种黄绿色刺激性气味的气体.这句话描述了氯气的物理性质(填“物理”或“化学”).能闻到氯气的刺激性气味,从微观的角度解释是B.
A.氯气具有很强的挥发性 B.氯气分子在不断运动
C.氯气分子是由氯原子构成的 D.氯气分子间存在间隙
(3)A、B、C、D表示四种物质,其微观示意图见下表.
| 物质 | A | B | C | D |  |
| 微观示意图 |  | 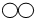 |  |  |
(4)对比、分析、归纳是学习化学的重要方法.
①已知H2、CO、C是初中化学常见的还原剂,请分析下列反应:
H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2
得出的结论是:物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合
价在反应后升高(选填“升高”或“降低”或“不变”).
②依据上述结论,则在反应SO2+2H2S=3S+2H2O中作为还原剂的物质是H2S;该还原剂中所含元素化合价的变化是:由-2价变为0价.
分析 (1)根据元素周期表每一小方格中的信息及原子结构示意图分析解答;元素周期表每一小方格下方数据表示相对原子质量,原子结构示意图中最外层电子数小于4个易失去电子显正价,多于4个易得到电子,显负价;周期数等于电子层数;
(2)依据物理性质的概念及特点结合分子的运动性分析判断即可;
(3)依据分子的结构判断分子的构成并书写相关的化学方程式,据此分析解答即可;
(4)氧化剂提供氧,化合价降低,具有氧化性,发生还原反应;还原剂得到氧,化合价升高,具有还原性,发生氧化反应.
解答 解:(1)元素周期表每一小方格下方数据表示相对原子质量,所以钠元素的相对原子质量为:22.99;氟元素原子最外层有7个电子,在形成化合物时易得到一个电子,显一1价,钠元素的原子最外层有1个电子,在形成化合物时易失去一个电子,显+1价,因此由氟元素和钠元素形成的化合物的化学式为NaF;D元素有三个电子层,应处于元素周期表中的第3周期.故答案为:22.99;NaF;3;
(2)物质的颜色、气味、密度和熔沸点等属于物质的物理性质,能闻到氯气的刺激性气味,由于分子的不断运动造成的;故填:物理;B;
(3)分析表中四种微粒的结构可知A、B、C、D四种物质的化学式,则A和B反应生成C和D的化学反应方程式是2H2S+O2$\frac{\underline{\;一定条件\;}}{\;}$2S+2H2O,所以A和B的分子个数比为2:1;
设若16gB参加反应,则生成D的质量是x
2H2S+O2$\frac{\underline{\;一定条件\;}}{\;}$2S+2H2O
32 36
16g x
$\frac{32}{36}=\frac{16g}{x}$
x=18g
故填:2:1;18;
(4)①在反应:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2中物质H2、CO、C做还原剂,其中氢元素和碳元素的化合价升高了,所以三个反应还原剂中元素的化合价的变化规律还原剂在化学反应中元素化合价升高;即可得出结论:物质作还原剂时,所含元素中,一定有元素的化合价在反应后升高;
②依据上述结论,则在反应SO2+2H2S═3S+2H2O中,H2S中硫元素的化合价由-2价升高到0价,所以H2S是还原剂.
故答案为:①升高;②H2S,-2,0.
点评 本题主要考查学生对课本知识掌握的熟练程度和总结规律的能力,属于基础知识的考查,对于化学方程式的考查是中考的一个重点.

(1)如图是某化学兴趣小组探究木炭燃烧条件的实验装置图:

该小组已经在完成气密性的检查后填装好了药品,并在整个装置中充满了氮气.请你继续完成实验并填写相应空格(要求实验过程中不得拆、装仪器).
| 步骤 | 操作 | 预计现象及得出的结论 |
| ① | 点燃酒精灯 | 木炭不燃烧,澄清石灰水未变浑,说明燃烧还需要氧气. |
| ② | 盖灭酒精灯,待仪器恢复到常温 | |
| ③ | 打开活塞,通入氧气 | 木炭不燃烧,澄清石灰水未浑浊,说明燃烧还需温度达到着火点. |
| ④ | 点燃酒精灯,继续通氧气 | 木炭燃烧,澄清石灰水变浑浊,说明燃烧需要同时具备上述两个条件才能生燃烧. |
(3)实验结束后,撤去酒精灯,木炭继续燃烧说明反应放热(填“放热”或“吸热”).
| A. | 胆矾 | B. | 无水硫酸铜 | C. | CuO | D. | NaCl |
步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明Na2CO3溶液显碱性;
步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含A.
(选填答案:A、稀盐酸 B、澄清石灰水 C、碳酸钠溶液)
【实验猜想】步骤3所得滤液中溶质可能为:
①NaCl、Na2CO3; ②NaCl、CaCl2和NaOH; ③NaCl、Na2CO3和NaOH; ④…
【实验验证】(提示:CaCl2溶液显中性)
| 实验操作 | 实验现象[] | 实验结论 |
| 取少量滤液于试管中,加入足量CaCl2溶液 | 猜想③成立 |

