题目内容
18.密度为1.84克/厘米3、质量分数为98%的浓硫酸1000毫升,可配制质量分数为20%的硫酸溶液9016克.分析 ①溶质质量与溶液质量的比值叫做溶质的质量分数,可用下式表示:溶质的质量分数=$;\frac{溶质质量}{溶液质量}\$$\frac{溶质质量}{溶液质量}$×100%;
②密度:某种物质单位体积的质量叫做这种物质的密度.用ρ表示密度,m表示质量,V表示体积,计算密度公式是ρ=$\frac{m}{v}$;
③由题意可知硫酸溶液稀释前后溶质的质量不变,然后根据这一等量关系列方程解答即可.
解答 解:根据溶液稀释前后溶质的质量不变得:
稀释前溶液的质量×稀释前溶质的质量分数=稀释后溶液的质量×稀释后溶质的质量分数
再由密度公式ρ=$\frac{m}{v}$得m=ρv
设可配制质量分数为20%的硫酸溶液为m,将数值代入公式,
得 1.84g/mL×1000mL×98%=m×20%
解得 m=9016g
答:可配制质量分数为20%的硫酸溶液9016克.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、稀释前后溶质的质量不变、量筒的使用方法等是正确解答本题的关键.

练习册系列答案
相关题目
6.保护环境、防止污染,人人应引起重视.下列反应的生成物不会污染空气的是( )
| A. | 点燃爆竹 | B. | 燃烧煤炭 | ||
| C. | 氢气通入氧化铜后加热 | D. | 氢气在氯气中燃烧 |
10.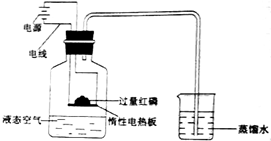 常温常压下,液态空气的沸点是-192℃,其简易获取过程:第一步:空气除尘净化,除去二氧化碳和水蒸气;第二步:在低温、高压的条件下,使空气液化,再用液态空气进行实验的装置如图:
常温常压下,液态空气的沸点是-192℃,其简易获取过程:第一步:空气除尘净化,除去二氧化碳和水蒸气;第二步:在低温、高压的条件下,使空气液化,再用液态空气进行实验的装置如图:
实验说明:电路开始处于断开状态,一旦接通电路,惰性电热板能起加热作用.
实验步骤及现象:
根据以上信息,回答下列问题:
(1)工业上制取液态空气时,常常需要将空气依次经过①液化器、②净化器、③压缩机等,你认为空气首先应经过②(选填①、②、③);
(2)请完善表格中的实验现象.
A烧杯中导管口不断产生气泡;
B导管中出现倒吸;
(3)步骤Ⅲ中,产生实验现象A的两个主要原因:①液态空气蒸腾产生大量的气体,该气体的主要成分是氮气;②装置内的压强不断增大;
(4)步骤Ⅳ中,红磷燃烧的化学符号表达式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
 常温常压下,液态空气的沸点是-192℃,其简易获取过程:第一步:空气除尘净化,除去二氧化碳和水蒸气;第二步:在低温、高压的条件下,使空气液化,再用液态空气进行实验的装置如图:
常温常压下,液态空气的沸点是-192℃,其简易获取过程:第一步:空气除尘净化,除去二氧化碳和水蒸气;第二步:在低温、高压的条件下,使空气液化,再用液态空气进行实验的装置如图:实验说明:电路开始处于断开状态,一旦接通电路,惰性电热板能起加热作用.
实验步骤及现象:
| 实验步骤 | 实验现象 |
| Ⅰ检查装置气密性,气密性良好 | -- |
| Ⅱ按装置要求连接好装置,并装好试剂 | 液态空气不断蒸腾,量不断减少,烧杯中导管口不断产生气泡 |
| Ⅲ一段时间后,接通电路 | 红磷不燃烧,烧杯中导管口不断产生气泡 |
| Ⅳ液态空气蒸发余下约十分之一时 | 红磷燃烧后,冒出大量白烟,放出大量热,… |
| Ⅴ红磷熄灭后,断开电路 | 白烟逐渐消失,导管中出现倒吸 |
(1)工业上制取液态空气时,常常需要将空气依次经过①液化器、②净化器、③压缩机等,你认为空气首先应经过②(选填①、②、③);
(2)请完善表格中的实验现象.
A烧杯中导管口不断产生气泡;
B导管中出现倒吸;
(3)步骤Ⅲ中,产生实验现象A的两个主要原因:①液态空气蒸腾产生大量的气体,该气体的主要成分是氮气;②装置内的压强不断增大;
(4)步骤Ⅳ中,红磷燃烧的化学符号表达式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
16.欲将100g溶质质量分数为10%的NaOH溶液变成质量分数为20%的NaOH溶液可采取的方法有( )
| A. | 加入100g 10%的NaOH溶液 | B. | 加入10g溶质 | ||
| C. | 蒸发掉45g水 | D. | 加入12.5g溶质 |
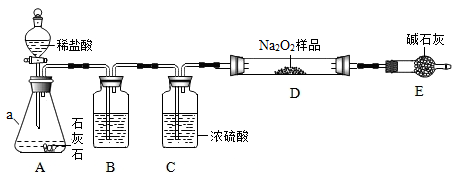
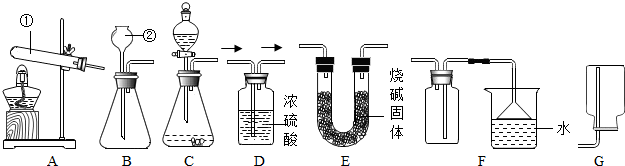
 小雨同学发现生活中铁在干燥的环境下很难生锈,而在潮湿的环境中却较易生锈,于是他认为有水铁就生锈,无水铁不生锈.为了证明自己结论的正确性,他设计了实验来验证.如图,他在A试管中盛市售新制蒸馏水,并将崭新铁片浸没于水中,上面滴入一层植物油;他将B试管烘干,放入同样铁片,并用橡皮塞封住管口. 分析:小雨在A试管中加入植物油的目的是隔绝氧气;放置一周后,结果他发现两只试管中铁片均未生锈,于是经过重新思考他改变了先前的观点,又得出了新结论铁与氧气和水共存时生锈;为了验证这个结论的正确性,他又增添了一套实验装置C,请你帮他画出此装置简图:又放置一周后,明显地观察到了铁锈,小雨终于得出了铁生锈的条件是与氧气、水共存.通过该实验探究,小雨同学获得了许多启示(请你写出一条)在设计实验探究时,方案要考虑全面,设计地要严密.
小雨同学发现生活中铁在干燥的环境下很难生锈,而在潮湿的环境中却较易生锈,于是他认为有水铁就生锈,无水铁不生锈.为了证明自己结论的正确性,他设计了实验来验证.如图,他在A试管中盛市售新制蒸馏水,并将崭新铁片浸没于水中,上面滴入一层植物油;他将B试管烘干,放入同样铁片,并用橡皮塞封住管口. 分析:小雨在A试管中加入植物油的目的是隔绝氧气;放置一周后,结果他发现两只试管中铁片均未生锈,于是经过重新思考他改变了先前的观点,又得出了新结论铁与氧气和水共存时生锈;为了验证这个结论的正确性,他又增添了一套实验装置C,请你帮他画出此装置简图:又放置一周后,明显地观察到了铁锈,小雨终于得出了铁生锈的条件是与氧气、水共存.通过该实验探究,小雨同学获得了许多启示(请你写出一条)在设计实验探究时,方案要考虑全面,设计地要严密.