题目内容
口子酒是我市的名特优产品,其独特的酒香主要来自于酿造和陈化过程中产生的乙酸乙酯(CH3COOC2H5),下列关于乙酸乙酯说法正确的是( )
|
| A. | 乙酸乙酯含有4个碳原子、8个氢原子、2个氧原子 |
|
| B. | 乙酸乙酯属于混合物 |
|
| C. | 乙酸乙酯中碳氢氧元素的质量比为2:4:1 |
|
| D. | 乙酸乙酯充分燃烧的产物只有CO2和H2O |
| 化学式的书写及意义;纯净物和混合物的判别;元素质量比的计算.. | |
| 专题: | 化学用语和质量守恒定律. |
| 分析: | A.根据乙酸乙酯的构成来分析; B.根据混合物和纯净物的概念来分析; C.根据化合物中各元素质量比的计算方法来分析; D.根据质量守恒定律来分析. |
| 解答: | 解:A.乙酸乙酯由乙酸乙酯分子构成,不是由碳、氢、氧三种原子构成,故错误; B.乙酸乙酯是由碳、氢、氧三种元素组成的化合物,不是混合物,故错误; C.由乙醇的化学式可知:乙醇中碳、氢、氧三种元素的质量比为(12×2):(1×6):16=12:3:8,不是2:4:1,故错误; D.乙酸乙酯中含有碳、氢、氧三种元素,根据质量守恒定律可知,其完全燃烧时产物只有水和二氧化碳两种物质,故正确. 故选D. |
| 点评: | 本题主要考查学生对化学式的意义的理解与掌握、根据化学式确定组成物质元素之间的质量关系进行解题的能力. |

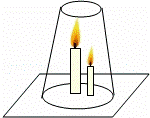
如图,将两支燃着的蜡烛罩上茶杯,过了一会儿高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑.由此我们可以得到启发:从着火燃烧的房间逃离时,下列做法中不正确的是( )
|
| A. | 用湿毛巾捂住鼻子 | B. | 成站立姿势跑出 |
|
| C. | 伏低身子逃出 | D. | 淋湿衣服爬出 |
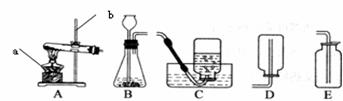
在实验操作考查中,小明抽到的题目是“二氧化碳的制取、收集和验满”.如图是他的主要实验步骤,其中操作有误的是( )
|
| A. |
加入药品 | B. |
收集气体 | C. |
检查装置气密性 | D. |
验满 |
钛(Ti)是广泛应用于航空、航海等领域的一种重要金属.在一定条件下,钛由四氯化钛(TiCl4)和金属镁反应而制得:TiCl4+2Mg═Ti+2MgCl2.现有380kg四氯化钛,可生产金属钛多少千克?
下列观点符合质量守恒定律的是( )
|
| A. | 煤燃烧后剩余残渣的质量减轻了 |
|
| B. | 一定条件下,SO2和O2生成SO3,反应前后分子总数不变 |
|
| C. | 8g CH4完全燃烧生成8g CO2 |
|
| D. | 某有机物在空气中燃烧只生成CO2和H2O,则该有机物一定含有碳、氢、氧元素 |
 、
、