题目内容
(8分)生活中常遇见铜制品生锈的情况。活动课上,同学们设计实验对铜锈进行了如下探究活动。
探究活动一:验证铜锈的组成
【查阅资料】
① 铜锈为绿色,其主要成分是Cu2(OH)2CO3。
② 白色的硫酸铜粉末遇水能变为蓝色。
③ 碳不与稀硫酸反应。
④ 氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液。
【进行实验1】
同学们设计了下图所示装置并进行实验。
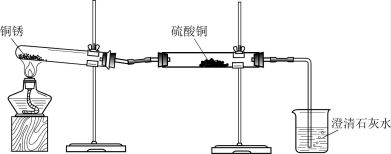
实验操作 | 实验现象 | 实验结论 |
① 按上图组装仪器,装入药品。 ② 加热铜锈,直至不再有气体产生,停止加热。 | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊。 | 加热铜锈生成的物质有_____;铜锈由_____元素组成;烧杯中发生反应的化学方程式为______。 |
③ 冷却后,向试管中固体加入适量稀硫酸,稍加热。 | 黑色固体溶解,溶液变为蓝色。 |
探究活动二:探究铜生锈的条件
【进行实验2】
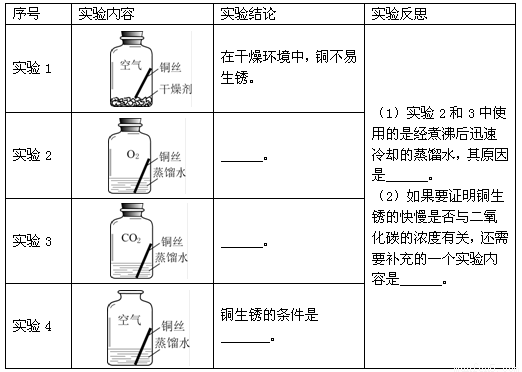
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显。
探究活动一:
CO2、H2O、CuO Cu、C、H、O CO2 + Ca(OH)2 == CaCO3↓+ H2O
探究活动二:
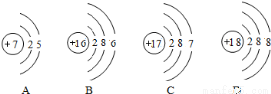
实验2:在有O2和H2O、无CO2 的环境中,铜不易生锈
实验3:在有CO2和H2O、无O2的环境中,铜不易生锈
实验4:与O2、CO2和H2O同时接触
(1)除去蒸馏水中溶解的O2和CO2
(2)按实验4内容重复操作后,再通入一定量的CO2排出部分空气,塞紧胶塞
【解析】
试题分析:加热铜锈生成的物质有CO2、H2O、CuO,烧杯中发生反应的化学方程式为二氧化碳和澄清的石灰水的反应,探究活动二意在验证铜生锈的条件,铜生锈必须和水,氧气 ,二氧化碳同时接触,否则不会生锈。
考点:铜锈的成分及其铜生锈的条件

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
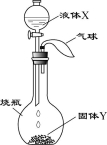
小博士期末闯关100分系列答案如图所示,将一定量的液体X滴入到烧瓶中,若使小气球鼓起(液体X的体积忽略不计),则液体X和固体Y不可能是
选项 | 液体X | 固体Y |
A | 水 | 氢氧化钠 |
B | 水 | 硝酸铵 |
C | 过氧化氢溶液 | 二氧化锰 |
D | 稀盐酸 | 碳酸钠 |
(7分)(1)小方用下图所示装置对二氧化碳的灭火实验进行研究,
实验的结论是______________________________________。
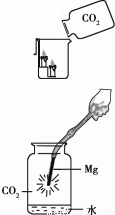
(2)【提出问题】二氧化碳能否支持燃烧?
【猜想假设】镁能在二氧化碳中燃烧。
【查阅资料】①氧化镁、氢氧化镁均是白色难溶于水的固体
②MgO+2HCl= MgCl2+H2O
③MgCl2+2NaOH=Mg(OH)2↓+2NaCl
【实验探究】
①上图中镁带剧烈燃烧,冒白烟,有黑色固体生成,并放出大量的热。
②为检验生成物的成分,做如下实验。
实验步骤 | 实验现象 | 实验结论和 化学方程式 | |
向广口瓶中加入过量盐酸,充分反应后过滤,在滤纸上留有黑色固体。 | I、将黑色固体收集、洗涤、干燥后,点燃,在火焰上方罩一个蘸有澄清石灰水的烧杯。 | 黑色固体燃烧,烧杯内壁出现白色浑浊。 | 黑色固体是 ; 涉及该步骤反应的化学方程式: 。 |
II、取少量滤液于试管中,逐滴加入氢氧化钠溶液。 | 有白色沉淀产生。 | 白烟的成分是 。 | |
③为了回收II中的白色沉淀,证明沉淀完全的实验方法是 。
(要求写出步骤、试剂、现象和结论)。
【反思提高】通过此次实验的探究,你对燃烧的条件或二氧化碳的灭火有何新认识 。
 ,请回答下列问题。
,请回答下列问题。