题目内容
通过对化学的学习,你已掌握了实验室制取气体的有关规律,请结合下图回答有关问题:
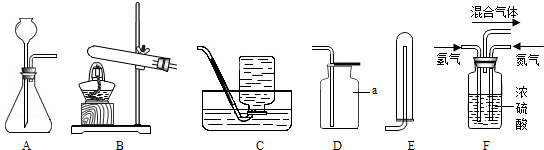
(1)图中标a的仪器名称是 .
(2)若实验室用加热氯酸钾的方法制取氧气,反应的化学方程式为 ,可选择的收集装置是D或 (填字母,下同).
(3)实验室用锌和稀硫酸制取氢气,应选择的发生装置是 ,
(4)氨气是一种无色、有刺激性气味、极易溶于水的气体,可用于制氮肥、硝酸、药物和染料等.
①若实验室用加热氯化铵和熟石灰的固体混合物的方法制取氨气,则实验室制取并收集氨气应选择的装置组合是 .
②工业上用氮气和氢气合成氨气.实验室模拟合成氨气的流程,流程中“气体的混合”是在F装置中进行的,F装置的作用有三个:一是将 干燥;二是使氮气和氢气充分混合;三是观察进气导管口逸出的气泡数,从而提高氮气和氢气的利用率.

(1)图中标a的仪器名称是
(2)若实验室用加热氯酸钾的方法制取氧气,反应的化学方程式为
(3)实验室用锌和稀硫酸制取氢气,应选择的发生装置是
(4)氨气是一种无色、有刺激性气味、极易溶于水的气体,可用于制氮肥、硝酸、药物和染料等.
①若实验室用加热氯化铵和熟石灰的固体混合物的方法制取氨气,则实验室制取并收集氨气应选择的装置组合是
②工业上用氮气和氢气合成氨气.实验室模拟合成氨气的流程,流程中“气体的混合”是在F装置中进行的,F装置的作用有三个:一是将
考点:常用气体的发生装置和收集装置与选取方法,气体的干燥(除水),实验室制取氧气的反应原理,氢气的制取和检验,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)熟悉常见仪器,了解名称;
(2)根据用氯酸钾制取氧气的反应物、反应条件、生成物写出化学方程式;根据氧气的密度和溶水性选择收集装置;
(3)根据锌和稀硫酸制取氢气,是固体和液体的不加热反应选择发生装置;
(4)①根据信息:氨气是一种无色、有刺激性气味、极易溶于水的气体,和用加热氯化铵和熟石灰的固体混合物的方法制取氨气.选择发生装置和收集装置;
②F装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是使氢气和氮气气流稳定.
(2)根据用氯酸钾制取氧气的反应物、反应条件、生成物写出化学方程式;根据氧气的密度和溶水性选择收集装置;
(3)根据锌和稀硫酸制取氢气,是固体和液体的不加热反应选择发生装置;
(4)①根据信息:氨气是一种无色、有刺激性气味、极易溶于水的气体,和用加热氯化铵和熟石灰的固体混合物的方法制取氨气.选择发生装置和收集装置;
②F装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是使氢气和氮气气流稳定.
解答:解:(1)图中a是集气瓶.故答案为:集气瓶.
(2)实验室用氯酸钾制取氧气,反应的化学方程式为2KClO3
2KCl+3O2↑.氧气的密度大于空气的密度,并且不易溶于水,所以用装置C或D收集.故答案为:2KClO3
2KCl+3O2↑;C.
(3)实验室用锌和稀硫酸制取氢气,该反应不需加热,属于固液常温型,故应选择的发生装置是A,故答案为:A;
(4)①根据信息:氨气是一种无色、有刺激性气味、极易溶于水的气体,和用加热氯化铵和熟石灰的固体混合物的方法制取氨气.可知是固体的加热反应,所以用装置B作发生装置;氨气的密度小于空气的密度,极易溶于水,所以收集装置用E.故答案为:BE;
②F装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是通过观察F中的气泡控制氮气和氢气的流量,使氢气和氮气气流稳定,达到最佳比例.故答案为:氮气和氢气.
(2)实验室用氯酸钾制取氧气,反应的化学方程式为2KClO3
| ||
| △ |
| ||
| △ |
(3)实验室用锌和稀硫酸制取氢气,该反应不需加热,属于固液常温型,故应选择的发生装置是A,故答案为:A;
(4)①根据信息:氨气是一种无色、有刺激性气味、极易溶于水的气体,和用加热氯化铵和熟石灰的固体混合物的方法制取氨气.可知是固体的加热反应,所以用装置B作发生装置;氨气的密度小于空气的密度,极易溶于水,所以收集装置用E.故答案为:BE;
②F装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是通过观察F中的气泡控制氮气和氢气的流量,使氢气和氮气气流稳定,达到最佳比例.故答案为:氮气和氢气.
点评:实验发生装置的选择要根据反应物的状态和反应条件,气体收集装置的选择要根据气体的密度和溶水性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
实验室用天平准确称量10.2g的食盐(1g以下用游码),发现称量时左物右码颠倒了,则实际称得的食盐的质量为( )
| A、10.2g | B、9.8g |
| C、10g | D、9.6g |