题目内容
15.推理是一种重要的学习方法,以下是某同学对所学化学知识的一些推理,其中合理的是( )| A. | 碳酸盐与稀盐酸反应能产生气体,所以与稀盐酸反应产生气体的物质一定是碳酸盐 | |
| B. | 碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液都是碱性溶液 | |
| C. | 燃烧一般都伴随发光、放热现象,所以有发光、放热现象的变化就是燃烧 | |
| D. | 中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应 |
分析 A、根据酸能与活泼金属、碳酸盐等反应生成气体,进行分析判断.
B、根据无色酚酞溶液遇碱性溶液变红色,进行分析判断.
C、根据燃烧的特征,进行分析判断.
D、中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水,进行分析判断.
解答 解:A、碳酸盐与稀盐酸反应能产生气体,所以与稀盐酸反应产生气体的物质不一定是碳酸盐,也可能是活泼金属等,故选项推理错误.
B、无色酚酞溶液遇碱性溶液变红色,碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液都是碱性溶液,故选项推理正确.
C、燃烧一般都伴随发光、放热现象,但有发光、放热现象的不一定就是燃烧,如灯泡发光放热,故选项推理错误.
D、中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,故选项推理错误.
故选:B.
点评 本题难度不大,掌握中和反应的特征、酸的化学性质、燃烧的特征等并能灵活运用是正确解答本题的关键.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
10.芬太奴是强有力的麻醉剂,在军事上作为“非致命武器”曾被用作解救人质,其化学式为C20H24N2O,下列关于芬太奴的说法中不正确的是( )
| A. | 芬太奴的每一个分子中含有47个原子 | |
| B. | 芬太奴是由碳、氢、氧、氮四种元素组成的物质 | |
| C. | 芬太奴中碳的质量分数最大 | |
| D. | 芬太奴中碳、氢、氧、氮的原子个数比为240:24:28:16 |
3.下列物品所使用的材料中,属于有机合成材料的是( )
| A. | 钛合金表链 | B. | 纯棉手套 | C. | 手机塑料外壳 | D. | 真丝围巾 |
20.下列说法中,不正确的是( )
| A. | 用量筒量取一定量的水,读数时要平视液体凹形液面中央最低处 | |
| B. | 制作糖水时候,用玻璃棒搅拌可以加快糖的溶解 | |
| C. | 在用烧杯配制氢氧化钠溶液时,将氢氧化钠溶于水,会感觉烧杯壁比较热 | |
| D. | 因为氯化钠没有腐蚀性,所以可以直接在托盘天平上称量 |
4.下列图象与变化关系正确的是( )
| A. | 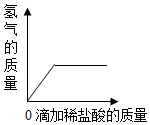 向一片久置于空气中的铝片样品滴加过量盐酸 | |
| B. | 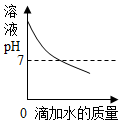 向一定质量的某碱溶液中逐渐滴加水 | |
| C. | 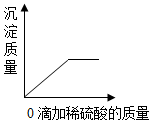 向硝酸钡溶液中滴加过量稀硫酸 | |
| D. | 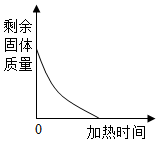 充分加热氯酸钾与二氧化锰的混合物制取氧气 |
5.向四只分别盛有稀硫酸的烧杯中不断加入下列物质,直至过量,最终溶液pH等于7的物质是( )
| A. | BaCl2 | B. | Mg(OH)2 | C. | NaOH | D. | Na2O |
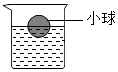 将一个塑料小球放入盛有AgNO3溶液的烧杯中,小球悬浮于液面,位置如图.将一定质量的铜片放入烧杯中,充分反应后(溶液的体积几乎不变),烧杯中出现哪些现象?写出发生的化学反应方程式.
将一个塑料小球放入盛有AgNO3溶液的烧杯中,小球悬浮于液面,位置如图.将一定质量的铜片放入烧杯中,充分反应后(溶液的体积几乎不变),烧杯中出现哪些现象?写出发生的化学反应方程式.