题目内容
15.在高温下用H2还原m克氧化铁,得到n克铁,氧的原子量为16,铁的原子质量是$\frac{24n}{m-n}$.分析 由化学方程式可以根据物质的实际质量来计算相对原子质量.
解答 解:设铁的相对原子质量为x.
3H2+Fe2O3 $\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O
x×2+16×3 x×2
mg ng
则$\frac{x×2+16×3}{x×2}=\frac{mg}{ng}$,解得x=$\frac{24n}{m-n}$
故答案为:
$\frac{24n}{m-n}$.
点评 本题主要考查有关化学方程式的常规计算,难度较小.

练习册系列答案
相关题目
5.互为同素异形体的一组物质是( )
| A. | 熟石灰和生石灰 | B. | 铁片和铁丝 | C. | 金刚石和石墨 | D. | 银和水银 |
3.在粗盐的初步提纯实验结束后,发现食盐产率偏低,原因可能是( )
| A. | 滤纸破损 | B. | 粗盐未充分溶解就过滤 | ||
| C. | 倾倒时有部分氯化钠溶液溅出 | D. | 蒸发后所得精盐潮湿 |
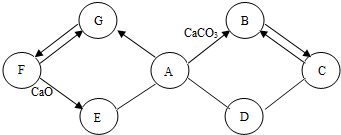
10.有一包白色固体A,可能含有FeCl3、CaCO3、NaOH、Ba(OH)2、BaCl2、Na2CO3中的一种或几种,取少量A做如下实验,现象如图所示.则下列说法正确的是


| A. | 白色固体A中一定不含有FeCl3 | |
| B. | 白色沉淀B一定是CaCO3,白色沉淀D一定是BaCO3 | |
| C. | 白色固体A如果是两种物质,则一定是CaCO3和Ba(OH)2 | |
| D. | 白色固体A可能是Na2CO3、BaCl2、NaOH的混合物 |
20.海水制镁时,有如下过程:海水$→_{①}^{加石灰乳}$$→_{②}^{过滤}$沉淀$→_{③}^{加盐酸}$$→_{④}^{蒸发}$氯化镁$→_{⑤}^{通电}$镁,对上述过程的认识错误的是( )
| A. | 通过过程①②③④,可得到纯净的MgCl2固体 | |
| B. | 过程②④属于物理变化 | |
| C. | 过滤后得到的沉淀时Mg(OH)2 | |
| D. | 海水中含有MgCl2,直接给海水通电也可得到镁 |
2.据2012年中央电视台3.15晚会报道:液化石油气掺入二甲醚(C2H6O)成行业潜规则,二甲醚对液化气罐的配件有腐蚀性,严重会造成爆炸.下列关于二甲醚的说法错误的是( )
| A. | 由C、H、O三种元素组成 | |
| B. | 相对分子质量46 | |
| C. | 是一种氧化物 | |
| D. | 碳、氢、氧三种元素的质量比为2:6:1 |