题目内容
12.将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如表:| 物质 | a | b | c | d |
| 反应前质量(g) | 6.4 | 3.2 | 4.0 | 0.5 |
| 反应后质量(g) | 待测 | 2.56 | 7.2 | 0.5 |
| A. | d可能是催化剂 | |
| B. | 反应后a物质的质量为4.64g | |
| C. | c物质中元素的种类,一定等于a、b二种物质中元素的种类 | |
| D. | a和b是反应物 |
分析 本题分析b、c、d三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定a是反应物还是生成物;根据各物质的质量变化情况结合催化剂、化合物的特征进行分析解答即可.
解答 解:根据质量守恒定律,由表中数据可知:b的质量减少了3.2g-2.56g=0.64g,可确定b是反应物;c的质量增加了7.2g-4.0g=3.2g,可确定c是生成物;d的质量反应前后不变;
A、d的质量不变,d可能作该反应的催化剂,也可能没有参加反应,故选项说法正确.
B、b的质量减少了是反应物,参加反应的b的质量为0.64g,生成物c的质量是3.2g,由质量守恒定律,a应是反应物,且参加反应的a的质量为3.2g-0.64g=2.56g故反应后a物质的质量为6.4g-2.56g=3.84g,故选项说法正不确.
C、根据分析,c物质中元素的种类一定等于a、b二种物质中元素的种类,故选项说法正确;
D、根据分析,a和b是反应物,故选项说法正确.
故选B.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
2.下述关于分子和原子的说法,正确的是( )
| A. | 在化学反应中,原子种类一定发生变化 | |
| B. | 同种原子可以结合成分子,不同种原子不能结合成分子 | |
| C. | 混合物与纯净物不同,纯净物只由一种原子组成 | |
| D. | 由分子构成的物质,分子是保持其化学性质的最小粒子 |
3.某物质在氧气中完全燃烧生成8.8g二氧化碳和5.4g水,关于这种物质组成的描述,正确的( )
| A. | 该物质只含有碳元素和氢元素 | |
| B. | 该物质中碳元素与氢元素的质量比为12:1 | |
| C. | 该物质一定含有碳元素、氢元素和氧元素 | |
| D. | 该物质的分子中碳原子和氢原子的个数比为1:3 |
17.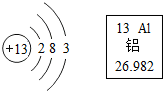 根据右图的信息判断,下列关于铝的说法错误的是( )
根据右图的信息判断,下列关于铝的说法错误的是( )
 根据右图的信息判断,下列关于铝的说法错误的是( )
根据右图的信息判断,下列关于铝的说法错误的是( )| A. | 属于金属元素 | |
| B. | 铝原子的核电荷数是13 | |
| C. | 相对原子质量是26.982 g | |
| D. | 在化学反应中,原子易失去电子形成Al3+ |
4.下列仪器中,不能直接加热的是( )
| A. | 量筒 | B. | 试管 | C. | 蒸发皿 | D. | 烧杯 |
1.化学用语是国际通用的化学语言,下列化学用语与含义相符的是( )
| A. | 2H2:4个氢原子 | |
| B. | Fe2+:一个铁离子带2个单位正电荷 | |
| C. | 2O:2个氧元素 | |
| D. | $\stackrel{+2}{CuO}$:氧化铜中铜元素的化合价为+2 |
2.下列物质在溶液中能大量共存且溶液为无色的是( )
| A. | 氢氧化钠 硫酸铁 氯化铵 | B. | 硝酸钠 氯化钡 氢氧化钙 | ||
| C. | 氢氧化钾 硫酸钠 硝酸铜 | D. | 稀硫酸 硝酸铵 氯化亚铁 |
