题目内容
8.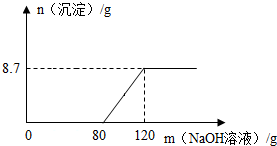 向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀与加入NaOH溶液的质量关系如图所示.
向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀与加入NaOH溶液的质量关系如图所示.(1)当加入NaOH溶液80g后,才开始有沉淀产生,原因是NaOH溶液先与硫酸,再与硫酸镁反应.
(2)计算氢氧化钠溶液的溶质质量分数.
分析 (1)根据开始没有沉淀生成,说明硫酸过量,NaOH溶液先与硫酸,再与硫酸镁反应进行解答;
(2)根据镁和稀硫酸反应生成硫酸镁和氢气,硫酸镁和氢氧化钠反应生成氢氧化镁沉淀,依据生成沉淀的质量计算消耗的氢氧化钠的质量;
解答 解:
(1)当加入NaOH溶液80g后,才开始有沉淀产生,原因是NaOH溶液先与硫酸,再与硫酸镁反应;
(2)由图示可知:当加入NaOH溶液80g后,才开始有沉淀产生,与硫酸镁反应的NaOH溶液的质量=120g-80g=40g
设与硫酸镁反应的NaOH的质量为x
2NaOH+MgSO4═Na2SO4+Mg(OH)2↓
80 58
x 8.7g
$\frac{80}{x}=\frac{58}{8.7g}$
x=12g
氢氧化钠溶液的溶质质量分数=$\frac{12g}{40g}×$100%=30%
答案:
(1)NaOH溶液先与硫酸,再与硫酸镁反应;
(2)氢氧化钠溶液的溶质质量分数为30%.
点评 本题主要考查学生利用化学方程式进行计算的能力.解题的关键是结合物质间反应的情况,正确分析图示数据,细心解答.

练习册系列答案
相关题目
17.中和反应在生活生产中有广泛的应用,下列做法不是利用中和反应原理的是( )
| A. | 用熟石灰改良酸性土壤 | B. | 用含氢氧化镁的药物治疗胃酸过多 | ||
| C. | 用盐酸除去铁锈 | D. | 用氨水(NH3•H2O)处理工厂的硫酸 |
16. 向一定质量氯化钙和稀盐酸的混合溶液中,逐滴加入一定质量分数的碳酸钠溶液,直至过量.某同学依据实验事实绘制了如图所示的曲线,下列说法正确的是( )
向一定质量氯化钙和稀盐酸的混合溶液中,逐滴加入一定质量分数的碳酸钠溶液,直至过量.某同学依据实验事实绘制了如图所示的曲线,下列说法正确的是( )
 向一定质量氯化钙和稀盐酸的混合溶液中,逐滴加入一定质量分数的碳酸钠溶液,直至过量.某同学依据实验事实绘制了如图所示的曲线,下列说法正确的是( )
向一定质量氯化钙和稀盐酸的混合溶液中,逐滴加入一定质量分数的碳酸钠溶液,直至过量.某同学依据实验事实绘制了如图所示的曲线,下列说法正确的是( )| A. | 实验中观察到现象是:先有白色沉淀后有气泡 | |
| B. | A至C段对应原来的溶液质量逐渐增加 | |
| C. | B至C段溶液的pH=7 | |
| D. | C点处溶液中溶质有NaCl和Na2CO3 |
13.下列实验操作正确的是( )
| A. | 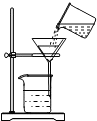 过滤 | B. | 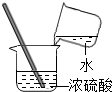 稀释浓硫酸 | ||
| C. | 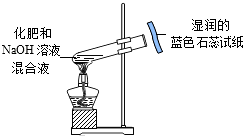 检验铵态氮肥 | D. | 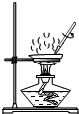 蒸发食盐水 |
20.正确的实验操作对实验结果,人身安全都非常重要,下列实验操作正确的是( )
| A. | 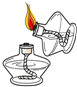 点燃酒精灯 | B. | 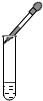 滴加液体 | C. | 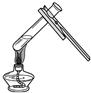 加热液体 | D. | 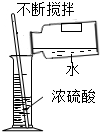 稀释浓硫酸 |
17.下列厨房中的物质溶于水能形成溶液的是( )
| A. | 面粉 | B. | 牛奶 | C. | 食用油 | D. | 蔗糖 |
18.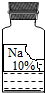 实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.
实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂溶质是什么?
【交流研讨】根据受损标签的情况判断,这瓶试剂不可能是A(填字母序号).
A. 酸 B.碱 C.盐
【查阅资料】①初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
②Na2CO3、NaHCO3溶液都呈碱性.NaCl溶液呈中性.
③室温下(20℃)时,4种物质的溶解度的数据如表一.
【得出结论】小华根据试剂瓶上标注和如表一溶解度数据判断,这瓶试剂不可能是NaHCO3.
【猜想与实验】①可能是Na2CO3溶液; ②可能是NaOH溶液; ③可能是NaCl溶液.
(1)小亮用洁净的玻璃棒蘸取该溶液,滴到干燥的pH试纸上,测得pH=11,他判断该溶液不可能是NaCl
(2)小强为了确定该溶液的成分,进行了如表二实验.
【质疑】小华则不同意小强的观点,认为溶液中有Na2CO3还可能有NaOH.请你帮助他完成以下探究方案:
 实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.
实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.【提出问题】这瓶试剂溶质是什么?
【交流研讨】根据受损标签的情况判断,这瓶试剂不可能是A(填字母序号).
A. 酸 B.碱 C.盐
【查阅资料】①初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
②Na2CO3、NaHCO3溶液都呈碱性.NaCl溶液呈中性.
③室温下(20℃)时,4种物质的溶解度的数据如表一.
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【猜想与实验】①可能是Na2CO3溶液; ②可能是NaOH溶液; ③可能是NaCl溶液.
(1)小亮用洁净的玻璃棒蘸取该溶液,滴到干燥的pH试纸上,测得pH=11,他判断该溶液不可能是NaCl
(2)小强为了确定该溶液的成分,进行了如表二实验.
| 操作步骤 | 实验现象 | 结论 |
| 步骤一:取样品于试管中,滴加足量稀盐酸 | 产生大量的气泡 | 猜想①正确. |
| 步骤二:把产生的气体,通入足量的澄清的石灰水中 | 石灰水变浑浊 |
| 探究步骤 | 预计现象 | 结论 |
| 步骤一:取样品于试管中,向其中滴加足量的BaCl2溶液并过滤 | 产生白色沉淀 | 溶液中既含Na2CO3,又含有NaOH |
| 步骤二:向上述滤液中滴加酚酞试液 | 酚酞试液变红色 |


