题目内容
10.用“○”和“●”分别代表两种不同元素的原子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如下,下列说法正确的是( )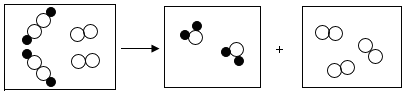
| A. | 该反应中反应物是一种单质和一种化合物 | |
| B. | 在反应中,两种生成物的分子个数比为2:3 | |
| C. | 符合该形式的化学方程式可以是2H2O2$\frac{\underline{\;通电\;}}{\;}$2H2O+O2↑ | |
| D. | 该反应的基本类型是置换反应 |
分析 A、对比反应前后分子的种类,根据构成相同的分子为同种物质的分子,判断反应前后物质种类;
B、根据反应前后分子的构成,对比反应前后原子种类、原子个数解答;
C、根据反应中反应物和生成物以及反应的条件书写反应的化学方程式
D、根据图示确定反应的类型;
解答 解:
根据图示可以看出,该反应的反应物是过氧化氢,生成物是水和氧气,化学方程式是::2H2O2$\frac{\underline{\;通电\;}}{\;}$2H2O+O2↑.
A、该反应中反应物是一种化合物,故错误;
B、在反应中,两种生成物的分子个数比为2:1,故错误;
C、该反应的反应物是过氧化氢,生成物是水和氧气,化学方程式是::2H2O2$\frac{\underline{\;通电\;}}{\;}$2H2O+O2↑.故正确;
D、该反应是一种物质生成了两种物质,属于分解反应,故错误.
答案:C
点评 本题考查了化学反应的微观模拟表示,完成此题,可以依据图示结合已有的知识进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列实验中,对应的现象及结论都正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 点燃纯净的甲烷 | 火焰呈蓝色 | 甲烷能支持燃烧 |
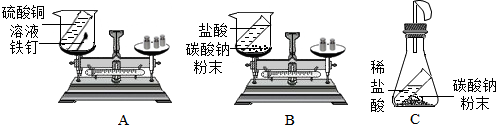
| B | 将铁丝和铜丝分别 放入稀盐酸中 | 铁丝表面有气泡产生, 铜丝表面无明显现象 | 铁的金属活动性比铜强 |
| C | 将硝酸铵溶于水 | 溶液温度降低 | 硝酸铵溶解放热 |
| D | 电解水 | 正极端玻璃管中产生的气体 体积比负极端玻璃管中的大 | 水是由氢、氧两种 元素组成的 |
| A. | A | B. | B | C. | C | D. | D |
1.将燃着的镁带伸入盛有二氧化碳集气瓶中,镁带继续剧烈燃烧,反应的化学方程式为:
2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,下列叙述错误的是( )
2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,下列叙述错误的是( )
| A. | 该反应中镁发生了氧化反应 | |
| B. | 该反应中元素的化合价都发生了改变 | |
| C. | 该反应说明了燃烧不一定都需要有氧气 | |
| D. | 镁着火时不能用二氧化碳灭火 |
18.用化学用语回答下列问题:
(1)三个亚铁离子3Fe2+;
(2)两个五氧化二磷分子2P2O5;
(3)过氧化氢中氢元素的化合价$\stackrel{+1}{H}$2O2;
(4)碳酸根离子CO32-.
(1)三个亚铁离子3Fe2+;
(2)两个五氧化二磷分子2P2O5;
(3)过氧化氢中氢元素的化合价$\stackrel{+1}{H}$2O2;
(4)碳酸根离子CO32-.
5.为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出).
【实验装置】
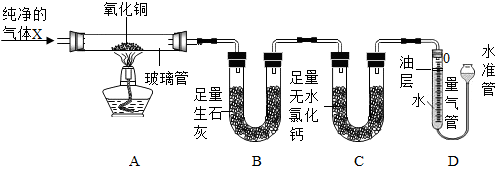
【查阅资料】
(1)加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
(2)生石灰与气体X不反应,无水氯化钙可吸收气体X.
(3)本实验条件下,装置内空气中的水、二氧化碳的影响可忽略不计.
【实验步骤】
(1)连接仪器,并检查装置气密性.
(2)准确称取2.40g氧化铜,装入A装置的玻璃管中,并在B、C、D中装入相应物质.
(3)测量并记录反应前的相关数据Ⅰ(见表).
(4)连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,再开始加热.(利用装置D中液面在反应前、后的刻度差,可测得生成的氮气的体积)
(5)当A装置中氧化铜反应完全后,停止加热,并继续通入气体X至玻璃管冷却.,再次测量并记录反应后的相关数据Ⅱ.
【相关数据】
注:如表中氮气的质量是通过D装置收集的氮气体积,并通过氮气的密度计算得到.
【回答问题】
(1)B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
(2)实验中,A装置的玻璃管中可观察到的现象是粉末由黑色逐渐变红.当观察到量气管内液面不再下降,说明氧化铜已完全反应.停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的铜被氧化.
(3)分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.
由此推知,气体X中没有(填“有”或“没有”或“可能有”)氧元素.
(4)气体X的化学式为NH3.
【实验装置】

【查阅资料】
(1)加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
(2)生石灰与气体X不反应,无水氯化钙可吸收气体X.
(3)本实验条件下,装置内空气中的水、二氧化碳的影响可忽略不计.
【实验步骤】
(1)连接仪器,并检查装置气密性.
(2)准确称取2.40g氧化铜,装入A装置的玻璃管中,并在B、C、D中装入相应物质.
(3)测量并记录反应前的相关数据Ⅰ(见表).
(4)连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,再开始加热.(利用装置D中液面在反应前、后的刻度差,可测得生成的氮气的体积)
(5)当A装置中氧化铜反应完全后,停止加热,并继续通入气体X至玻璃管冷却.,再次测量并记录反应后的相关数据Ⅱ.
| 数据编号 测量项目 | Ⅰ | Ⅱ |
| 玻璃管(含药品)的质量/g | 54.40 | 53.92 |
| B装置(含药品)的质量/g | 104.00 | 104.54 |
| 氮气的质量/g | / | 0.28 |
注:如表中氮气的质量是通过D装置收集的氮气体积,并通过氮气的密度计算得到.
【回答问题】
(1)B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
(2)实验中,A装置的玻璃管中可观察到的现象是粉末由黑色逐渐变红.当观察到量气管内液面不再下降,说明氧化铜已完全反应.停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的铜被氧化.
(3)分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.
由此推知,气体X中没有(填“有”或“没有”或“可能有”)氧元素.
(4)气体X的化学式为NH3.
2.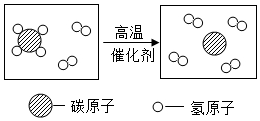 如图是某反应的微观示意图,下列说法正确的是( )
如图是某反应的微观示意图,下列说法正确的是( )
 如图是某反应的微观示意图,下列说法正确的是( )
如图是某反应的微观示意图,下列说法正确的是( )| A. | 该反应是分解反应 | |
| B. | 分子是化学变化中最小的粒子 | |
| C. | 反应前后原子种类发生改变 | |
| D. | 该反应的化学方程式为CH4+2H2$→_{催化剂}^{高温}$C+4H2↑ |