题目内容
7.请根据如图所示的实验室中实验装置图填空.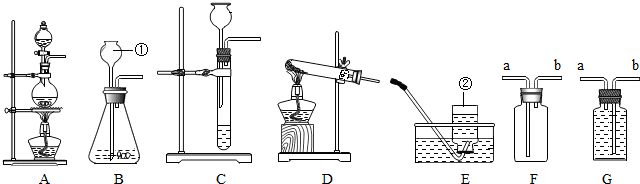
(1)完成图中标有数字的仪器的名称:①长颈漏斗 ②集气瓶
(2)用高锰酸钾制备氧气选择D装置,写出反应化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)在实验室中,制取并收集二氧化碳选用装置为B和F(填字母编号),反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(4)实验室制得的CO2气体中常含有水蒸气.为了得到纯净、干燥的CO2气体,除杂装置的导管气流方向连接顺序是A(填选项 A.a→b B.b→a).
(5)有一名同学欲用F装置收集H2,则H2应从导管口b 通入;若用G来收集一瓶O2,则O2应从导管口a通入.
(6)已知MnO2固体和浓盐酸混合共热可制得氯气(Cl2),则应选用A做气体发生装置.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大;
(4)浓硫酸可以用来干燥二氧化碳;
(5)氢气密度比空气小,氧气不易溶于水;
(6)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
解答 解:(1)①是长颈漏斗,②是集气瓶.
故填:长颈漏斗;集气瓶.
(2)用高锰酸钾制备氧气需要加入,应该选择D装置,反应化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
故填:D;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)在实验室中,制取二氧化碳不需要加入,应该用B装置作为发生装置;
二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用F装置收集;
反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故填:B;F;CaCO3+2HCl═CaCl2+H2O+CO2↑.
(4)实验室制得的CO2气体中常含有水蒸气,为了得到纯净、干燥的二氧化碳气体,除杂装置的导管气流方向连接顺序是a→b.
故填:A.
(5)欲用F装置收集氢气,由于氢气密度比空气小,则氢气应从导管口b通入;
若用G来收集一瓶氧气,则氧气应从导管口a通入.
故填:b;a.
(6)已知二氧化锰固体和浓盐酸混合共热可制得氯气,则应选用A做气体发生装置.
故填:A.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案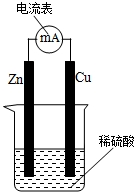
| 电极 | 碳棒-铜片 | 碳棒-铁片 | 碳棒-锌片 |
| 电流强度(mA) | 1.43 | 4.26 | 4.63 |
| 电压(V) | 0.6 | 1.2 | 1.3 |
(1)上述装置中能量的转变是从化学能转变为电能.该实验经过一段时间后溶液pH的变化是增大(选填“增大”“减小”或“不变”).
(2)假如仅改用镁片和碳棒做电极,其它实验条件不变,根据上表的实验数据,你猜想产生的电压应比表中三种电池产生的电压都大(选填“都大”、“都小”、“处在它们之间”或“无法判断”).
(3)将三个用碳棒和锌片做电极的单个水果电池串联起来,将铭牌为“2.5V 0.3A”的一个小灯泡串联接入该电路,开关闭合后,小灯泡并不正常发光,原因是水果电池电压太低(或电流太小).
| A. | 水→氢气+氧气 | B. | 木炭+氧化铜→铜+二氧化碳 | ||
| C. | 氢气+氧气→水 | D. | 氧化汞→汞+氧气 |
 甲、乙两固体物质的溶解度曲线如图,下列说法不正确的是( )
甲、乙两固体物质的溶解度曲线如图,下列说法不正确的是( )| A. | t1℃时,甲的饱和溶液中溶质的质量分数为20% | |
| B. | 随着温度的升高,甲的溶解度增大,乙的溶解度减小 | |
| C. | t2℃时,甲、乙两种物质的溶解度相等 | |
| D. | t1℃时可通过升温将接近饱和的乙溶液转成饱和溶液 |
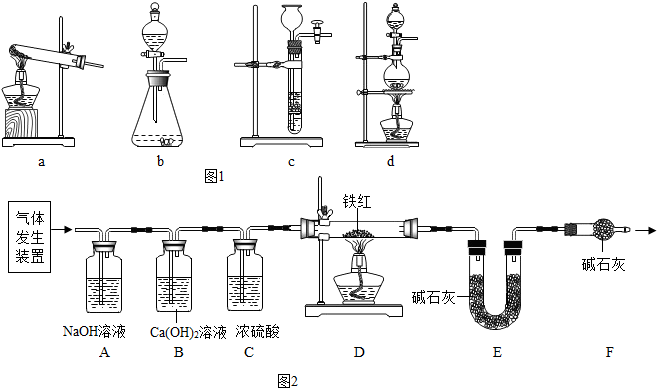
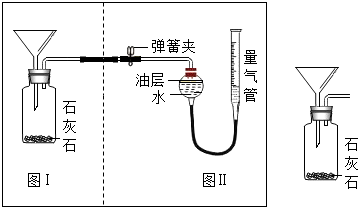 石灰石是一种重要矿石,其主要成分为碳酸钙,在冶金、建材、化工等行业均有广泛用途.某校9年级科学探究小组的同学为了测定某种石灰石样品中碳酸钙的质量分数,设计了如下实验方案:取一定质量的石灰石样品与足量稀盐酸反应,测量反应后生成的CO2的体积,再将体积换算成质量,最后根据CO2的质量计算样品中碳酸钙的质量分数.下图Ⅰ为石灰石与稀盐酸反应的装置,图Ⅱ为测量CO2体积的装置.
石灰石是一种重要矿石,其主要成分为碳酸钙,在冶金、建材、化工等行业均有广泛用途.某校9年级科学探究小组的同学为了测定某种石灰石样品中碳酸钙的质量分数,设计了如下实验方案:取一定质量的石灰石样品与足量稀盐酸反应,测量反应后生成的CO2的体积,再将体积换算成质量,最后根据CO2的质量计算样品中碳酸钙的质量分数.下图Ⅰ为石灰石与稀盐酸反应的装置,图Ⅱ为测量CO2体积的装置.