题目内容
课外小组同学利用如图所示装置制取二氧化碳,并对其性质进行研究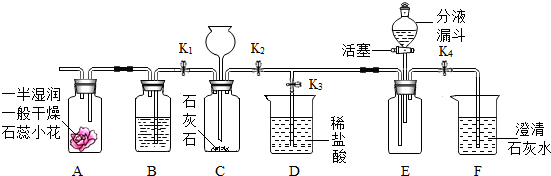
友情提示:使用分液漏斗时,可通过开启、关闭活塞控制液体的流入,同时防止装置漏气.
(1)若打开止水夹K1,关闭K2,从长颈漏斗向装置C中加入足量的稀盐酸,C中发生反 应的化学方程式为 .通过分析A中的现象可证明CO2具有的性质是 .B中盛放的试剂是 .
(2)若打开止水夹K2、K4,关闭K1、K3,从长颈漏斗向装置C中加入足量的稀盐酸,当观察到 的现象时,证明E中CO2已集满.关闭止水夹K2、K4,打开K3,从分液漏斗向E中加入适量的氢氧化钠溶液.该实验中,能证明CO2与NaOH确实发生了化学反应的现象是 .

友情提示:使用分液漏斗时,可通过开启、关闭活塞控制液体的流入,同时防止装置漏气.
(1)若打开止水夹K1,关闭K2,从长颈漏斗向装置C中加入足量的稀盐酸,C中发生反 应的化学方程式为
(2)若打开止水夹K2、K4,关闭K1、K3,从长颈漏斗向装置C中加入足量的稀盐酸,当观察到
考点:二氧化碳的实验室制法,二氧化碳的化学性质,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:综合实验题
分析:(1)石灰石的主要成分是碳酸钙,和盐酸反应生成氯化钙、水和二氧化碳,据此书写方程式;二氧化碳能与水反应生成碳酸,碳酸可使石蕊变红,要证明二氧化碳和水反应,A中放的是一半湿润一半干燥的石蕊小花进行对比,则进入的二氧化碳应是干燥的,避免水蒸气的干扰,所以B中应放浓硫酸对气体加以干燥;
(2)二氧化碳能使澄清的石灰水变浑浊,盐酸和碳酸钠反应生成二氧化碳,并结合装置分析.
(2)二氧化碳能使澄清的石灰水变浑浊,盐酸和碳酸钠反应生成二氧化碳,并结合装置分析.
解答:解:(1)石灰石的主要成分是碳酸钙,和盐酸反应生成氯化钙、水和二氧化碳,方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳能与水反应生成碳酸,碳酸可使石蕊变红,则A中会观察到湿润的湿润试纸变红,而干燥的试纸不变色,从而说明二氧化碳能与水反应;要证明二氧化碳和水反应,A中用的是一半湿润一半干燥的石蕊小花进行对比,则进入的二氧化碳应是干燥的,避免水蒸气的干扰,所以B中应放浓硫酸对气体加以干燥;
(2)二氧化碳能使澄清的石灰水变浑浊,E装置是用向上排空气法收集,所以若F中澄清的石灰水变浑浊,说明E中二氧化碳已收集满;关闭止水夹K2、K4,打开K3,随着二氧化碳的增多,则D中的稀盐酸会进入E装置,二氧化碳和氢氧化钠反应生成碳酸钠,而碳酸钠和盐酸反应生成二氧化碳,与氢氧化钠反应生成氯化钠和水,所以从分液漏斗向E中加入适量的氢氧化钠溶液,若观察到气泡冒出,则说明二氧化碳和氢氧化钠确实发生了反应;
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳能与水反应; 浓硫酸;
(2)F中石灰水变浑浊; E中有气泡冒出.
(2)二氧化碳能使澄清的石灰水变浑浊,E装置是用向上排空气法收集,所以若F中澄清的石灰水变浑浊,说明E中二氧化碳已收集满;关闭止水夹K2、K4,打开K3,随着二氧化碳的增多,则D中的稀盐酸会进入E装置,二氧化碳和氢氧化钠反应生成碳酸钠,而碳酸钠和盐酸反应生成二氧化碳,与氢氧化钠反应生成氯化钠和水,所以从分液漏斗向E中加入适量的氢氧化钠溶液,若观察到气泡冒出,则说明二氧化碳和氢氧化钠确实发生了反应;
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳能与水反应; 浓硫酸;
(2)F中石灰水变浑浊; E中有气泡冒出.
点评:本题能很好的考查学生对知识的掌握和应用,分析、解决问题的能力,是一道不错的题目.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
能够一次性把澄清石灰水,烧碱溶液,盐酸鉴别开的试剂是( )
| A、碳酸钠溶液 | B、石蕊溶液 |
| C、酚酞试液 | D、硫酸铜溶液 |
下列做法错误的是( )
| A、食酸奶能促进食物消化 |
| B、用灯帽盖熄酒精灯火焰 |
| C、用钛镍合金制卫星天线 |
| D、工业上不可以用食盐为原料来制取碳酸钠 |
有一包固体粉末,可能由CaCO3、Na2SO4、KNO3、CuSO4、BaCl2中的一种或几种组成,做实验得以下结果:(1)将此固体粉末加到水中,得到白色沉淀,且上层清液为无色;(2)该白色沉淀部分溶于稀硝酸,并有无色气体产生.据此实验,得出的下列判断中正确的是( )
| A、该粉末中一定含有CaCO3、Na2SO4、BaCl2 |
| B、该粉末中一定不含有KNO3、CuSO4 |
| C、该粉末中一定含有KNO3 |
| D、该粉末中一定含有Na2SO2、KNO3、BaCl2 |
下列物质的化学式中,书写正确的是( )
| A、硝酸铜 CuNO3 |
| B、氯化铁FeCl2 |
| C、氢氧化镁MgOH |
| D、氧化铝Al2O3 |
 今年冬季我市出现了严重的雾霾天气,标志性建筑索菲亚教堂已模糊不清.
今年冬季我市出现了严重的雾霾天气,标志性建筑索菲亚教堂已模糊不清.