题目内容
6.钠及其化合物是中学化学学习和研究的重要内容.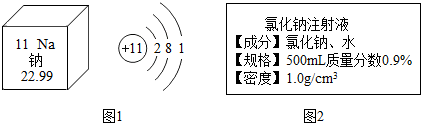
(1)如图是钠元素在周期表中的信息和钠原子结构示意图,下列是某同学从如图获得的信息,其中错误的是bc(填标号).
a.钠属于金属元素 b.钠的相对原子质量为22.99g
c.钠原子在化学反应中易得到电子 d.
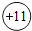 表示原子核带11个单位正电荷
表示原子核带11个单位正电荷(2)钠可以与水发生反应:2Na+2H2O=2NaOH+X↑,则X的化学式为O2.
(3)配制一瓶如图2所示的溶液,请问:①需要称取氯化钠的质量为4.5g,需加入水的体积为495.5ml②若用6%氯化钠溶液加水稀释而成,则需6%氯化钠溶液的质量75g.
(4)碳酸氢钠受热易分解生成碳酸钠,水和二氧化碳,写出该反应的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O↑;用化学方法鉴别碳酸氢钠和氯化钠两种白色固体的方法是取少量样品,加入稀盐酸,有气体产生的则是碳酸氢钠,无明显变化的则是氯化钠(包括实验步骤,现象和结论).
分析 (1)根据钠元素原子结构示意图和在周期表中的信息,进行解答.
(2)根据质量守恒定律:反应前后,原子种类、数目均不变,和反应的化学方程式2Na2O2+2H2O═4NaOH+X↑,进行推测X的化学式.
(3)根据溶液中的相关计算方法来分析;
(4)根据方程式的写法以及物质的性质来分析.
解答 解:(1)a.钠属于金属元素,故说法正确;
b.最下面的数值是相对原子质量,因此钠元素的相对原子质量是22.99,故说法错误;
c.钠原子的最外层电子数少于4个,在反应中容易失去1个电子,故错误;
d.原子核带11个单位的正电荷,故正确;
故选bc;
(2)根据反应的化学方程式2Na2O2+2H2O═4NaOH+X↑,反应物中Na、H、O原子个数分别为4、4、6,反应后的生成物Na、H、O原子个数分别为4、4、4,根据反应前后原子种类、数目不变,则X中含有2个O原子,则物质X的化学式为O2;故填:O2;
(3)溶质的质量=溶液的体积×溶液的密度×溶质的质量分数=500mL×1.0g/mL×0.9%=4.5g;需水:500mL×1.0g/mL-4.5g=495.5g,即495.5mL水;故填:4.5;495.5;
设需要6%的氯化钠溶液的质量为x,则x×6%=4.5g
x=75g
故填:75;
(4)碳酸氢钠分解可以得到碳酸钠、二氧化碳和水,反应的方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O↑.
碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳,氯化钠与盐酸不反应,所以可以用稀盐酸来鉴别;故填:取少量样品,加入稀盐酸,有气体产生的则是碳酸氢钠,无明显变化的则是氯化钠.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法、对原子结构示意图及其意义的理解,明确元素周期表中元素的信息人含义、原子结构示意图中最外层电子数与得失电子的关系是解题的关键.

①用520的白酒和紫包菜制取酸碱指示剂
②用碎鸡蛋壳和食醋制取少量CO2
③用纯碱溶液制取叶脉书签
④用果汁、白糖、水、柠檬酸、小苏打等自制汽水.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
| A. | 氧气液化变为淡蓝色液体 | |
| B. | 二氧化碳通入紫色的石蕊试液,试液变为红色 | |
| C. | 碘溶于酒精得到棕黄色溶液 | |
| D. | 高锰酸钾稀释后变为浅紫红色 |
| A. | 力推火力发电 | B. | 节日燃放烟花 | C. | 露天焚烧垃圾 | D. | 机动车限号行驶 |
 铁锅是生活中常用的炊具,如图是某铁锅的示意图.
铁锅是生活中常用的炊具,如图是某铁锅的示意图. 宜春温汤的富硒盐皮蛋因含硒而被大家熟知,皮蛋中含有丰富的蛋白质、脂肪、维生素和铁、钙、钾等人体所需要的矿物质元素.
宜春温汤的富硒盐皮蛋因含硒而被大家熟知,皮蛋中含有丰富的蛋白质、脂肪、维生素和铁、钙、钾等人体所需要的矿物质元素.
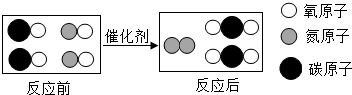 如图是某反应的微观示意图.图中的单质为氮气,该反应前后化合价没有发生变化的元素为氧元素.
如图是某反应的微观示意图.图中的单质为氮气,该反应前后化合价没有发生变化的元素为氧元素.