题目内容
6.在学习盐的化学性质时,老师将一定量的碳酸钠溶液与氯化钙溶液混合,过滤反应后的混合物.老师要求同学们探究滤液中溶质的组成.请你一同参与探究并回答有关问题.【查阅资料】碳酸钠溶液显碱性,氯化钠、氯化钙溶液显中性.
【提出猜想】
猜想1:滤液中溶质是NaCl;
猜想2:滤液中溶质是NaCl和CaCl2的混合物(填化学式);
猜想3:滤液中溶质是NaCl和Na 2CO3的混合物.
猜想4:滤液中溶质是NaCl、Na2CO3和CaCl2的混合物.
你认为上述猜想4有错误,理由是碳酸钠和氯化钙不能共存.
【实验探究】
(1)取少量滤液于试管中,滴加2-3滴无色酚酞试液,振荡,无明显现象.同学们认为猜想3不成立.
(2)另取少量滤液于另一支试管中,滴加碳酸钠溶液,若有白色沉淀产生(填实验现象),证明猜想2成立.
【问题讨论】
小红同学认为要证明猜想2成立也可以改用硝酸银溶液.你认为小红同学不能(填“能”或“不能”)达到实验目的.理由是氯化钠和氯化钙都能和硝酸银反应生成生成白色沉淀氯化银.
分析 【提出猜想】
碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠;
【实验探究】
显碱性的溶液能使酚酞试液变红色;
【问题讨论】
氯化钠和硝酸银反应生成白色沉淀氯化银和硝酸钠;
氯化钙和硝酸银反应生成白色沉淀氯化银和硝酸钙.
解答 解:【提出猜想】
碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,如果恰好完全反应,滤液中的溶质是氯化钠,如果碳酸钠过量,滤液中的溶质是氯化钠和碳酸钠,如果氯化钙过量,滤液中的溶质是氯化钠和氯化钙;
上述猜想4有错误,理由是碳酸钠和氯化钙不能共存.
故填:CaCl2;4;碳酸钠和氯化钙不能共存.
【实验探究】
(1)取少量滤液于试管中,滴加2-3滴无色酚酞试液,振荡,无明显现象,说明溶液中不含有碳酸钠,即猜想3不成立.
故填:3.
(2)另取少量滤液于另一支试管中,滴加碳酸钠溶液,若产生白色沉淀,证明猜想2成立.
故填:白色沉淀产生.
【问题讨论】
因为氯化钠和氯化钙都能和硝酸银反应生成生成白色沉淀氯化银,所以要证明猜想2成立,不能改用硝酸银溶液.
故填:不能;氯化钠和氯化钙都能和硝酸银反应生成生成白色沉淀氯化银.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
16.2008年9月27日我国航天员成功完成了太空漫步.2011年9月29日,天宫一号也发射升空,中华民族千年飞天梦圆.为解决航天员的呼吸问题,舱外航天服应能提供的物质是( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 水 |
17.下列说法中正确的是( )
| A. | 水是由两个氢元素和一个氧元素组成的 | |
| B. | 水是由氢和氧两种元素组成的 | |
| C. | 水是由氢和氧两种单质组成的 | |
| D. | 水分子是由氢分子和氧分子构成的 |
3.请将下列化学符号中数字“2”表示的意义在下表中寻找对应的位置,然后填上其序号.
①2CO②Ca2+③H2 ④$\stackrel{+2}{Fe}$SO4
①2CO②Ca2+③H2 ④$\stackrel{+2}{Fe}$SO4
| 表示分子个数 | ① | 表示离子所带电荷数 | ② |
| 表示元素化合价 | ④ | 表示分子中原子的个数 | ③ |
10.如图表示M、N两种固体物质的溶解度曲线,下列对图示信息的描述正确的是( )
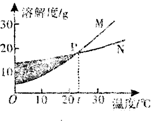

| A. | 30℃时M的溶解度小于N的溶解度 | |
| B. | 分离M、N可采用蒸发结晶的方法 | |
| C. | M、N都是难溶物质 | |
| D. | 阴影处各点对应的溶液(不包含曲线上的点)是N的不饱和溶液,M的饱和溶液 |
8.以下物质的用途主要是由其化学性质决定的是( )
| A. | 干冰可用于冷藏食品 | B. | 氧气用于帮助呼吸 | ||
| C. | 活性炭用于除去冰箱中的异味 | D. | 石墨用于做电极 |
 我在路边的围墙上看到一则化肥广告(如图):回校后,我通过计算氮的质量分数发现该广告是虚假广告.我认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现其氮元素质量分数仅为12.0%,我能算出该产品中碳酸氢铵的质量分数为67.8%.
我在路边的围墙上看到一则化肥广告(如图):回校后,我通过计算氮的质量分数发现该广告是虚假广告.我认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现其氮元素质量分数仅为12.0%,我能算出该产品中碳酸氢铵的质量分数为67.8%.