题目内容
经科学研究发现,元素原子如果最外层电子数是4,其单质在导电方面具有某些特殊的优良性能,如硅原子最外电子层电子数为4,常用作半导体材料.下列可作半导体材料的是( )
A、铝 Al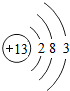 |
B、氧 O 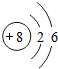 |
C、锗 Ge 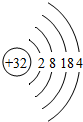 |
D、氖 Ne 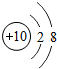 |
考点:核外电子在化学反应中的作用
专题:化学用语和质量守恒定律
分析:根据题意,元素原子如果最外层电子数是4,其单质在导电方面具有某些特殊的优良性能,如硅原子最外电子层电子数为4,常用作半导体材料;据此可知,可作半导体材料的是,其原子的最外电子层电子数为4,进行分析判断即可.
解答:解:元素原子如果最外层电子数是4,其单质在导电方面具有某些特殊的优良性能,如硅原子最外电子层电子数为4,常用作半导体材料;则可作半导体材料的是,其原子的最外电子层电子数为4.
A、该原子的最外层电子数为3,不符合要求,故选项错误.
B、该原子的最外层电子数为6,不符合要求,故选项错误.
C、该原子的最外层电子数为4,符合要求,故选项正确.
D、该原子的最外层电子数为8,不符合要求,故选项错误.
故选:C.
A、该原子的最外层电子数为3,不符合要求,故选项错误.
B、该原子的最外层电子数为6,不符合要求,故选项错误.
C、该原子的最外层电子数为4,符合要求,故选项正确.
D、该原子的最外层电子数为8,不符合要求,故选项错误.
故选:C.
点评:本题难度不大,理解元素原子如果最外层电子数是4常用作半导体材料是正确解答本题的关键.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
下列各种物质间的转换通过一步反应不能实现的是( )
| A、H2SO4→H2O |
| B、Cu→Cu(OH)2 |
| C、Fe→FeCl2 |
| D、CO2→CO |
推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论.以下推理正确的是( )
| A、氧化物中含有氧元素,含氧元素的化合物一定是氧化物 |
| B、离子是带电荷的微粒,带电荷的微粒一定是离子 |
| C、H2SO4溶液能使石蕊溶液变红,使石蕊溶液变红的溶液一定是H2SO4溶液 |
| D、碱性溶液在常温下pH>7,测定某溶液的pH=12,则该溶液一定呈碱性 |
下列化学方程式符合题意且书写正确的是( )
A、用点燃的方法除去二氧化碳中少量的一氧化碳:2CO+O2
| ||||
| B、证明铁的活动性比银强:Fe+2AgCl═FeCl2+2Ag | ||||
| C、医疗上用氢氧化铝中和过多胃酸:2Al(OH)3+3 H2SO4═Al2(SO4)3+6H2O | ||||
D、用一氧化碳还原氧化铁:Fe2O3+3CO
|