题目内容
11.某同学利用实验室准备好的固体食盐、水以及一些相应的仪器配制50g5%的食盐溶液,下列说法正确的是( )| A. | 所用仪器有:托盘天平、试管、烧杯、玻璃棒 | |
| B. | 实验中玻璃棒的作用是加快溶解 | |
| C. | 量取水时仰视液面读数 | |
| D. | 称量时左盘放2g砝码,游码移至0.5g处 |
分析 A、根据配制溶液时所需的仪器判断;
B、根据配制溶液时玻璃棒的作用判断;
C、根据量筒的正确使用方法判断;
D、根据天平的使用要遵循“左物右码”的原则判断.
解答 解:A、配制溶液时所需的仪器:托盘天平(砝码) 烧杯 玻璃棒 胶头滴管 量筒 药匙等,不需试管,故A错误;
B、在溶解过程中玻璃棒的作用是搅拌,加速溶解,故B正确;
C、用量筒量取液体时,读数时视线与凹液面的最底处保存水平,不可俯视,也不可仰视,故C错误;
D、天平的使用要遵循“左物右码”的原则,左盘不可放砝码,故D错误.
故选B.
点评 本题主要考查了一定质量分数的溶液的配制.配制一定溶质质量分数的溶液,一般要经过计算、称量(或量取)、溶解(或稀释)、装瓶存放等步骤.

练习册系列答案
相关题目
2. 工业用碳酸钠溶液与石灰水反应制烧碱.对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究.
工业用碳酸钠溶液与石灰水反应制烧碱.对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究.
提出假设:
假设一:滤液中只含氢氧化钠
假设二:滤液中含氢氧化钠和氢氧化钙
假设三:滤液中含氢氧化钠和碳酸钠
假设四:滤液中含氢氧化钠、氢氧化钙和碳酸钠
甲同学设计了如表实验方案:
已知:Na2CO3+CaCl2═2NaCl+CaCO3↓(白色),试回答:
(1)写出碳酸钠溶液与石灰水反应的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)哪种假设不合理,试说明理由假设四不合理,因为氢氧化钙溶液与碳酸钠溶液不能共存.
(3)乙同学认为甲同学设计方案还不能说明碳酸钠溶液和澄清石灰水恰好完全反应,她的理由是若氢氧化钙过量与氯化钙不发生反应.
(4)丙同学认为要说明碳酸钠溶液与石灰水是否恰好完全反应,还需在甲同学实验方案的基础上增加一个实验.她的实验方案是:
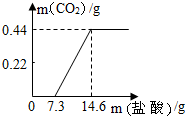
(5)取18.6g氢氧化钠样品(样品中的杂质是碳酸钠),加水溶解得到溶液A,取A溶液的$\frac{1}{10}$向其中逐滴加入一定浓度的稀盐酸,并同时记录放出CO2的质量和消耗盐酸的质量(所得数据如图).请完成下列任务:
①写出如图中ab段发生反应的化学方程式NaOH+HCl═NaCl+H2O.
②样品中碳元素的质量分数为6.5%.(结果保留到0.1%)
 工业用碳酸钠溶液与石灰水反应制烧碱.对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究.
工业用碳酸钠溶液与石灰水反应制烧碱.对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究.提出假设:
假设一:滤液中只含氢氧化钠
假设二:滤液中含氢氧化钠和氢氧化钙
假设三:滤液中含氢氧化钠和碳酸钠
假设四:滤液中含氢氧化钠、氢氧化钙和碳酸钠
甲同学设计了如表实验方案:
| 实验步骤 | 实验现象 | 结论 |
| 取少量滤液放在试管中,再滴入氯化钙溶液 | 若生成白色沉淀 | 碳酸钠过量 |
| 若无明显现象 | 恰好反应 |
(1)写出碳酸钠溶液与石灰水反应的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)哪种假设不合理,试说明理由假设四不合理,因为氢氧化钙溶液与碳酸钠溶液不能共存.
(3)乙同学认为甲同学设计方案还不能说明碳酸钠溶液和澄清石灰水恰好完全反应,她的理由是若氢氧化钙过量与氯化钙不发生反应.
(4)丙同学认为要说明碳酸钠溶液与石灰水是否恰好完全反应,还需在甲同学实验方案的基础上增加一个实验.她的实验方案是:
| 实验步骤 | 实验现象和结论 |
①写出如图中ab段发生反应的化学方程式NaOH+HCl═NaCl+H2O.
②样品中碳元素的质量分数为6.5%.(结果保留到0.1%)
19.有关水的认识正确的是( )
| A. | 电解水得到H2和O2,说明水是由氢元素和氧元素组成的 | |
| B. | 利用沉淀、过滤、吸附、电解等方法可以净化水 | |
| C. | 生活中用过滤的方法可以降低水的硬度 | |
| D. | 物质溶于水所得到的溶液是均一、稳定、无色、透明的 |
6.2016年,“3.15”国际消费者权益日主题为“新消费.我做主”,央视“3.15”晚会对国内各行各业存在的侵犯消费者权益的行为进行了集体曝光,合理利用化学物质会提高生活质量,下列有关做法中,正确的是( )
| A. | 用亚硝酸盐代替食盐烹调食物 | |
| B. | 适量碳酸氢钠用于治疗胃酸过多 | |
| C. | 用工业石膏或医疗废弃石膏制作豆腐 | |
| D. | 少量甲醛用于海鲜的保鲜 |
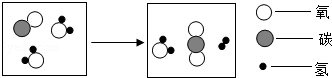 如图表示在一定条件下,物质转化过程的微观示意图,请根据图形信息回答问题:
如图表示在一定条件下,物质转化过程的微观示意图,请根据图形信息回答问题: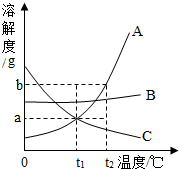 如图是A、B、C三种物质的溶解度曲线,请根据此图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,请根据此图回答下列问题: