题目内容
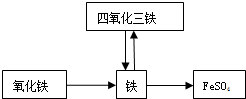 如图是铁的知识网络图(反应条件已略),用化学用语填空:
如图是铁的知识网络图(反应条件已略),用化学用语填空:(1)铁中铁元素的化合价
(2)高炉炼铁的原理
考点:金属的化学性质,铁的冶炼,化学符号及其周围数字的意义,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)依据化学用语的有关要求分析解决;
(2)根据高炉炼铁的原理是一氧化碳把铁从铁矿石里还原出来分析;
(2)根据高炉炼铁的原理是一氧化碳把铁从铁矿石里还原出来分析;
解答:解:(1)铁是单质,其中铁元素的化合价为0;硫酸亚铁中亚铁离子是阳离子,硫酸根是阴离子,其符号为SO42-.铁转化为硫酸亚铁,一般规律是铁参与的置换反应会出现该转化,所以铁与稀硫酸制氢气,铁与硫酸铜反应置换出铜均会生成硫酸亚铁.方程式为Fe+H2SO4═FeSO4+H2↑或Fe+CuSO4═Cu+FeSO4;
(2)高炉炼铁的原理是一氧化碳把铁从铁矿石里还原出来,如果是赤铁矿则方程式为:Fe2O3+3CO
2Fe+3CO2.
故答案为:(1)0;SO42-;Fe+H2SO4═FeSO4+H2↑或Fe+CuSO4═Cu+FeSO4;
(2)Fe2O3+3CO
2Fe+3CO2.
(2)高炉炼铁的原理是一氧化碳把铁从铁矿石里还原出来,如果是赤铁矿则方程式为:Fe2O3+3CO
| ||
故答案为:(1)0;SO42-;Fe+H2SO4═FeSO4+H2↑或Fe+CuSO4═Cu+FeSO4;
(2)Fe2O3+3CO
| ||
点评:本题侧重考查物质间的相互转化及化学用语,因此要求同学们熟悉物质间的相互反应,要放开思维,从多方面,多角度考虑问题答案.

练习册系列答案
相关题目
下列关于空气的说法中,不正确的是( )
| A、空气是混合物 |
| B、稀有气体可做保护气 |
| C、氮气约占空气体积分数的78% |
| D、空气中的有毒气体为:CO2SO2 NO2 |
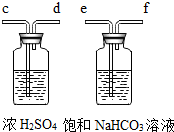 除去物质中混有杂质的原则是:不能引入新的杂质,还要注意不能与待提纯物质反应、除杂成本、回收等因素,常用物理方法和化学方法除杂.
除去物质中混有杂质的原则是:不能引入新的杂质,还要注意不能与待提纯物质反应、除杂成本、回收等因素,常用物理方法和化学方法除杂.