题目内容
7.金属盒金属材料在生活、生产中应用广泛.(1)铁在潮湿的空气中容易生锈,实际上是与空气中的氧气、水等发生了化学反应;
(2)用Fe、Ag和②溶液(填序号),可以一次性验证Fe、Cu、Ag三种金属的活动性顺序,写出有关反应的化学方程式Fe+CuSO4=Cu+FeSO4.
①AgNO3溶液 ②CuSO4溶液 ③Al2(SO4)3溶液.
分析 根据铁生锈的条件以及金属活动性顺序的意义进行分析解答即可.
解答 解:(1)铁在与水和氧气并存时易生锈,故填:氧气,水;
(2)要验证铁、铜银的金属活动性,可以采取两金夹一盐的方法,故可以选择硫酸铜溶液,铁能与硫酸铜溶液反应生成硫酸亚铁和铜,故填:②,Fe+CuSO4=Cu+FeSO4.
点评 本题考查的是金属的有关性质以及金属活动性顺序的应用的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
18.每年的5月13 日是世界无烟日,香烟的成分很复杂,燃烧产生的烟气中含有许多强致癌物质和有害物质,其中对人体危害最大的分别是尼古丁(化学式为C10H14N2)、焦油、一氧化碳等,下列说法错误的是( )
| A. | 吸烟严重危害身心健康 | |
| B. | 尼古丁中碳、氢、氧三种元素质量比为60:7:14 | |
| C. | 尼古丁中含有10个碳原子,14个氢原子和2个氮原子 | |
| D. | 一氧化碳能与血液里的血红蛋白结合,故而有剧毒 |
15.下列实验现象或实验原理正确的是( )
| A. | 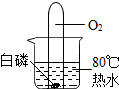 白磷始终不燃烧 | B. | 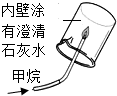 验证甲烷燃烧生成二氧化碳和水 | ||
| C. | 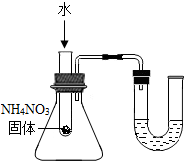 U形管内液面左高右低 | D. | 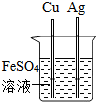 验证Fe、Cu、Ag的金属或定性强弱 |
2.下列关于反应的描述,反应方程式及反应类型完全正确的是( )
| A. | 小苏打受热分解:NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O 化合反应 | |
| B. | 铁丝在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 分解反应 | |
| C. | 检验食盐中存在氯离子:NaCl+AgNO3═NaNO3+AgCl↓ 复分解反应 | |
| D. | 将铁片投入足量的稀盐酸中:2Fe+6HCl═2FeCl3+3H2↑ 置换反应 |
12.某校化学兴趣小组同学在实验室整理药品时,发现氢氧化钠溶液的试剂瓶未塞瓶塞,且试剂瓶口周围有一些白色固体,他们怀疑氢氧化钠已经变质,于是进行了如下实验探究.
【提出问题】氢氧化钠溶液是否变质?
【查阅资料】氯化钠溶液、氯化钡溶液呈中性.
【实验探究】小王、小李两同学分别设计了不同方案并加以实验.
(1)小李同学认为小王同学的结论不科学,其理由是Na2CO3溶液也显碱性,即使NaOH变质,溶液的pH也大于7.
(2)小李同学的实验中观察到实验现象A为产生白色沉淀,该反应的化学方程式为Na2CO3+BaCl2=2NaCl+BaCO3↓.
【拓展应用】
(3)若要除去上述变质的氢氧化钠溶液中的杂质应加入适量的Ba(OH)2(填化学式)溶液而除去.
【提出问题】氢氧化钠溶液是否变质?
【查阅资料】氯化钠溶液、氯化钡溶液呈中性.
【实验探究】小王、小李两同学分别设计了不同方案并加以实验.
| 实验步骤 | 实验现象 | 结论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 说明氢氧化钠溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | A | 说明氢氧化钠溶液已经变质 |
(2)小李同学的实验中观察到实验现象A为产生白色沉淀,该反应的化学方程式为Na2CO3+BaCl2=2NaCl+BaCO3↓.
【拓展应用】
(3)若要除去上述变质的氢氧化钠溶液中的杂质应加入适量的Ba(OH)2(填化学式)溶液而除去.
17.下列实验方法不能达到实验目的是( )
| A. | 除去粗盐中的难溶性杂质--将粗盐溶解、过滤、蒸发 | |
| B. | 除去CO中的CO2---通入足量的氢氧化钠溶液 | |
| C. | 除去热水瓶胆中的水垢--用食醋 | |
| D. | 鉴别稀盐酸、氢氧化钠溶液、氯化钠溶液--滴加无色酚酞溶液 |