题目内容
2.兴趣小组为探究CO2的相关性质,设计了以下实验:在体积相同的两个集气瓶中装满CO2,并装上与大气相通的气球,分别从注射器中注入等体积的澄清石灰水和氢氧化钠溶液,实验现象如图1.(1)甲装置中发生的现象是澄清石灰水变浑浊,气球变大,说明产生了新物质;
(2)乙装置中气球变大,小刚认为CO2与氢氧化钠发生了反应,小明认为不一定,理由是二氧化碳不但能与氢氧化钠反应还能与水反应,不能证明二氧化碳与氢氧化钠发生了反应,为此设计了如下实验,实验现象如图2所示:
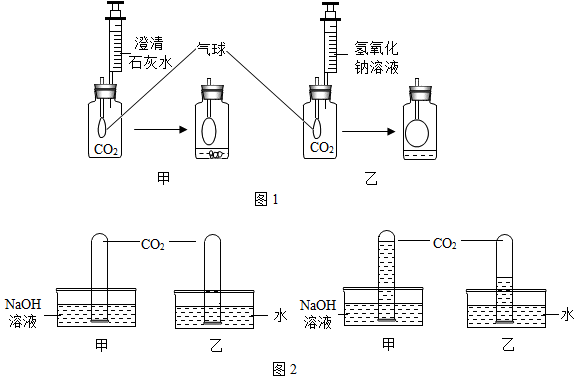
(3)小红认为通过对比甲、乙装置中气球的变化情况,不能说明氢氧化钠吸收CO2的能力更强.她的理由是注入等体积的澄清石灰水和氢氧化钠溶液,没有注明浓度无法比较.
分析 (1)二氧化碳与氢氧化钙反应生成碳酸钙和水,
(2)二氧化碳不但能与氢氧化钠反应还能与水反应,不能证明二氧化碳与氢氧化钠发生了反应;
(3)根据氢氧化钙和氢氧化钠的溶解性分析.
解答 解:(1)甲装置中二氧化碳与石灰水反应生成碳酸钙沉淀,澄清石灰水变浑浊,集气瓶中二氧化碳减少,压强变小,气球变大.
(2)二氧化碳不但能与氢氧化钠反应还能与水反应,不能证明二氧化碳与氢氧化钠发生了反应;应将氢氧化钠溶液换成等体积的水来与实验对比.
(3)由于氢氧化钙是微溶,氢氧化钠是易溶,注入等体积的澄清石灰水和氢氧化钠溶液,没有注明浓度无法比较.
故答案为:(1)澄清石灰水变浑浊,气球变大;(2)二氧化碳不但能与氢氧化钠反应还能与水反应,不能证明二氧化碳与氢氧化钠发生了反应;
(3)注入等体积的澄清石灰水和氢氧化钠溶液,没有注明浓度无法比较.
点评 解答本题要充分理解各种物质的性质方面的知识,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案
相关题目
17.将一定量的酒精(学名乙醇)和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水蒸汽和一种未知物X.测得反应前后物质的质量如下表:
下列判断错误的是( )
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.4 | 5.4 | m |
| A. | 表中m的值为2.8 | |
| B. | X中氧元素的质量为1.6g | |
| C. | 增加氧气的量可以减少X的生成 | |
| D. | 物质X一定含有1.2g碳元素,可能含有氢元素 |
18.在小组活动中,老师讲烘干的碳酸镁与锌粉按照一定比例研细混匀,按照图1进行实验.
【提出问题】碳酸镁与锌粉反应的产物是什么?
【查阅资料】①氧化镁、氧化锌:均为白色固体,均与盐酸反应,生成无色盐溶液.
②碳酸镁、碳酸锌:均为白色固体,均与盐酸反应,生成无色盐溶液和二氧化碳气体.
【实验探究】
(1)实验一:碳酸镁与锌粉反应的气体产物是什么?
结论:碳酸镁与锌粉反应的气体燃烧的化学方程式为2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
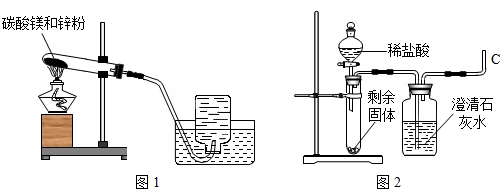
2)实验二:碳酸镁与锌粉反应的固体产物是什么?
老师将加热后的剩余固体分成两份,由甲、乙两组同学进行探究.
甲组同学将剩余固体直接按照图2进行实验,观察到A中有大量气泡生成,B中的澄清石灰水变浑浊,将产生的气体在C处验纯后点燃,观察到淡蓝色火焰.C处点燃的气体是H2(填化学式).甲组同学获得结论:该反应的固体产物是碳酸锌和镁.
乙组同学提出了质疑,他们先将另一份剩余固体先进行了处理,然后也按照图2进行了实验,观察到A中固体溶解,生成无色溶液,B中没有明显变化.他们对剩余固体的处理操作是继续按图1方式加热,直至不再产生气体.乙组同学利用实验现象,分析碳酸镁与锌粉反应的化学方程式为MgCO3+Zn$\frac{\underline{\;\;△\;\;}}{\;}$MgO+ZnO+CO↑.甲组同学对实验过程再次进行了认真分析,确定他们放入试管A中的固体含有MgCO3、Zn、MgO、ZnO.
【实验反思】:通过以上实验说明,在研究反应后的产物时.要考虑反应物是否有剩余.
【提出问题】碳酸镁与锌粉反应的产物是什么?
【查阅资料】①氧化镁、氧化锌:均为白色固体,均与盐酸反应,生成无色盐溶液.
②碳酸镁、碳酸锌:均为白色固体,均与盐酸反应,生成无色盐溶液和二氧化碳气体.
【实验探究】
(1)实验一:碳酸镁与锌粉反应的气体产物是什么?
| 序号 | 实验操作 | 实验现象 |
| ① | 收集两瓶气体,盖好玻璃片,停止加热,向其中一瓶迅速倒入少量澄清石灰水,盖好振荡. | 无明显现象. |
| ② | 将另一瓶气体点燃,待火焰熄灭后,迅速倒入少量澄清石灰水,盖好振荡. | 气体安静燃烧,火焰呈蓝色,澄清石灰水变浑浊. |

2)实验二:碳酸镁与锌粉反应的固体产物是什么?
老师将加热后的剩余固体分成两份,由甲、乙两组同学进行探究.
甲组同学将剩余固体直接按照图2进行实验,观察到A中有大量气泡生成,B中的澄清石灰水变浑浊,将产生的气体在C处验纯后点燃,观察到淡蓝色火焰.C处点燃的气体是H2(填化学式).甲组同学获得结论:该反应的固体产物是碳酸锌和镁.
乙组同学提出了质疑,他们先将另一份剩余固体先进行了处理,然后也按照图2进行了实验,观察到A中固体溶解,生成无色溶液,B中没有明显变化.他们对剩余固体的处理操作是继续按图1方式加热,直至不再产生气体.乙组同学利用实验现象,分析碳酸镁与锌粉反应的化学方程式为MgCO3+Zn$\frac{\underline{\;\;△\;\;}}{\;}$MgO+ZnO+CO↑.甲组同学对实验过程再次进行了认真分析,确定他们放入试管A中的固体含有MgCO3、Zn、MgO、ZnO.
【实验反思】:通过以上实验说明,在研究反应后的产物时.要考虑反应物是否有剩余.
15.某同学对所学的部分化学知识归纳如下,其中完全正确的一组是( )
| 化肥的种类、鉴别及使用 | 化学应用 | ||
A | CO(NH2)2、(NH4)2SO4和NaNO3均可用作氮肥 从外观上可区分硫酸钾和磷矿粉两种肥料 给农作物施肥时同时施用草木灰和碳酸氢铵以提高肥效 | B | 用肥皂水检验硬水和软水 用食醋清洗家用瓷器上的水垢 用燃烧后闻气味的方法鉴别衣服面料是蚕丝还是合成纤维涤纶 |
| 食品安全 | 能源与环境 | ||
C | 用硫磺熏制白木耳、粉丝等食品 用小苏打作焙制糕点的发酵粉 除鱼胆汁苦味(酸性)--纯碱溶液浸泡 | D | 煤、石油燃烧--无污染 车用乙醇汽油--减少污染 氢能--无污染 |
| A. | A | B. | B | C. | C | D. | D |
7.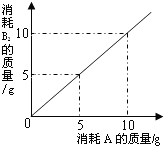 在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,将5gA与8gB2充分反应,则生成AB2的质量是( )
在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,将5gA与8gB2充分反应,则生成AB2的质量是( )
 在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,将5gA与8gB2充分反应,则生成AB2的质量是( )
在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,将5gA与8gB2充分反应,则生成AB2的质量是( )| A. | 10g | B. | 13g | C. | 16g | D. | 18g |
14.元素X的原子结构示意图为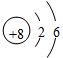 ,下列说法不正确的是( )
,下列说法不正确的是( )
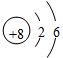 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | X的常见单质的化学式可表示为X2 | |
| B. | X的常见单质具有可燃性 | |
| C. | 酒精在X的常见单质中燃烧生成CX2和H2X | |
| D. | 在人体组织里,葡萄糖在酶的催化作用下跟X的常见单质反应产生共机体活动和维持恒定体温的能量 |