题目内容
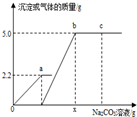 向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )| A、图中Oa段表示生成沉淀的过程 |
| B、x值为106.0 |
| C、c点溶液的pH<7 |
| D、b点溶液中溶质有2种 |
考点:盐的化学性质,溶液的酸碱性与pH值的关系
专题:常见的盐 化学肥料
分析:由图象分析可知:图中Oa段表示生成气体二氧化碳的过程,已知二氧化碳是2.2g,根据Na2CO3→CO2可计算需要碳酸钠的质量是5.3g,即碳酸钠溶液的质量=5.3g÷10.0%=53g;根据生成沉淀的质量是5g,Na2CO3→CaCO3可计算需要碳酸钠的质量是5.3g,即碳酸钠溶液的质量=5.3g÷10.0%=53g,因此x=53g+53g=106.0g;c点是碳酸钠溶液过量,因为碳酸钠呈碱性,因此溶液的pH>7;b点是恰好完全反应的点,溶液中只有氯化钠一种溶质.
解答:解:A、图中Oa段表示生成气体二氧化碳的过程,不是沉淀,故选项错误;
B、已知二氧化碳是2.2g,根据Na2CO3→CO2可计算需要碳酸钠的质量是5.3g,即碳酸钠溶液的质量=5.3g÷10.0%=53g;根据生成沉淀的质量是5g,Na2CO3→CaCO3可计算需要碳酸钠的质量是5.3g,即碳酸钠溶液的质量=5.3g÷10.0%=53g,因此x=53g+53g=106.0g;故选项正确;
C、c点是碳酸钠溶液过量,因为碳酸钠呈碱性,因此溶液的pH>7,故选项错误;
D、b点是恰好完全反应的点,溶液中只有氯化钠一种溶质,故选项错误;
故选B
B、已知二氧化碳是2.2g,根据Na2CO3→CO2可计算需要碳酸钠的质量是5.3g,即碳酸钠溶液的质量=5.3g÷10.0%=53g;根据生成沉淀的质量是5g,Na2CO3→CaCO3可计算需要碳酸钠的质量是5.3g,即碳酸钠溶液的质量=5.3g÷10.0%=53g,因此x=53g+53g=106.0g;故选项正确;
C、c点是碳酸钠溶液过量,因为碳酸钠呈碱性,因此溶液的pH>7,故选项错误;
D、b点是恰好完全反应的点,溶液中只有氯化钠一种溶质,故选项错误;
故选B
点评:本考点属于盐的化学性质和有关的计算,盐的化学性质有四个:盐与金属反应、盐与酸反应、盐与碱反应、盐与盐反应.解决本考点需要根据图象,综合分析,从而得出正确的结论.此考点主要出现在选择题、和实验题中.

练习册系列答案
相关题目
下列元素符号和名称,书写不完全正确的是( )
| A、P 磷 |
| B、mg 镁 |
| C、Zn 锌 |
| D、Cu 铜 |
配制10%的氢氧化钠溶液100mL,应选用的仪器是( )
①量筒②酒精灯③玻璃棒④蒸发皿⑤烧杯⑥天平.
①量筒②酒精灯③玻璃棒④蒸发皿⑤烧杯⑥天平.
| A、①②③⑥ | B、①②④⑤ |
| C、①③⑤⑥ | D、①②③④ |
下列变化在厨房中经常发生,其中属于物理变化的是( )
| A、液化气燃烧 | B、铁锅生锈 |
| C、开水沸腾 | D、蔬菜腐烂 |
下列符号既能表示一种元素,又能表示一个原子,还能表示一种单质的是( )
| A、H2 |
| B、H |
| C、Al3+ |
| D、Ag |
下列有关碳和碳的氧化物的说法中不正确的是( )
| A、金刚石、石墨和C60都是由碳元素组成的单质 |
| B、一氧化碳能与血液中的血红蛋白结合,导致中毒 |
| C、金刚石和石墨的结构中碳原子的排列方式不同 |
| D、二氧化碳不能与水发生反应 |
密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法不正确的是( )
| 物 质 | A | B | C | D |
| 反应前质量/g | 10 | 10 | 10 | 10 |
| 反应后质量/g | 待测 | 12 | 12 | 3 |
| A、反应后密闭容器中A的质量为13g |
| B、该反应一定是分解反应 |
| C、物质D一定是化合物 |
| D、反应生成的A与B的质量之比为13:12 |
下列实验操作或作法正确的是( )
| A、用100mL量筒量取8.5mL的水 |
| B、为了不造成浪费,实验剩余的药品放回原瓶 |
| C、把烧杯放在垫有石棉网的铁圈上加热 |
| D、用燃着的酒精灯去点燃另一酒精灯 |
 图为A、B、C在水中的溶解度曲线图:
图为A、B、C在水中的溶解度曲线图: