题目内容
5.欲除去NaNO3溶液中含有的少量Ag+、Ca2+应先加入适量氯化钠溶液,过滤后再加入适量碳酸钠溶液,再过滤最终得到硝酸钠溶液.分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:硝酸钠中混有硝酸银和硝酸钙,其中的杂质离子分别是银离子和钙离子,这两种离子需要分别转化为氯化银沉淀和碳酸钙沉淀而除去,因此可以加入氯化钠和碳酸钠,为避免碳酸钠的加入产生碳酸银沉淀,因此先加入氯化钠除去硝酸银,再加入碳酸钠除去硝酸钙,然后过滤就得到硝酸钠溶液;
故答案为:氯化钠;碳酸钠;硝酸钠.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
14.同学们进入初三了,除了用“洪荒之力”好好拼搏一年外!还要讲学习方法.学习化学需要运用科学的方法,下列选项中不属于学习化学的方法是( )
| A. | 进行化学实验 | B. | 进行科学探究 | C. | 使用化学符号 | D. | 使用占卜手段 |
15. 溶解度可表示物质溶解性的大小.
溶解度可表示物质溶解性的大小.
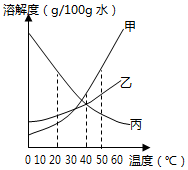
(1)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.
①20℃时,甲的溶解度<(填“>”、“<”或“=”)乙的溶解度.
②40℃时,乙和丙能(填“能”或“不能”)形成溶质质量分数相同的饱和溶液.
③20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃.请填写下表.
(2)气体的溶解度也有一定的变化规律:
打开可乐瓶,逸出大量气泡.由此可见,压强越小,CO2的溶解度越小.为增大CO2的溶解度,可采用的一种方法是增大压强或降低温度.
 溶解度可表示物质溶解性的大小.
溶解度可表示物质溶解性的大小.(1)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.
①20℃时,甲的溶解度<(填“>”、“<”或“=”)乙的溶解度.
②40℃时,乙和丙能(填“能”或“不能”)形成溶质质量分数相同的饱和溶液.
③20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃.请填写下表.
| 烧杯中的溶质 | 烧杯中固体的变化 |
| 甲 | 固体逐渐全部溶解 |
| 乙 | 固体逐渐部分溶解 |
| 丙 | 固体逐渐固体不溶解,反而增多 |
打开可乐瓶,逸出大量气泡.由此可见,压强越小,CO2的溶解度越小.为增大CO2的溶解度,可采用的一种方法是增大压强或降低温度.
 能与对面
能与对面 中能反应的为同伴,硫酸找同伴1,同伴1找同伴2,同伴2找同伴3,见图.
中能反应的为同伴,硫酸找同伴1,同伴1找同伴2,同伴2找同伴3,见图.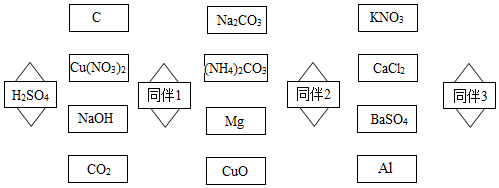
 如图是为探究物质燃烧条件设计的实验(热水的温度超过白磷着火点).
如图是为探究物质燃烧条件设计的实验(热水的温度超过白磷着火点).