题目内容
将10g含氧64%的CO和CO2的混合物,依次通过足量灼热的CuO、足量澄清的石灰水,得到的沉淀质量为 .(假设每步反应完全)
考点:质量守恒定律及其应用,化合物中某元素的质量计算,混合物中某元素的质量计算
专题:化学用语和质量守恒定律
分析:由题意“10g含氧64%的CO和CO2的混合物”,则碳元素的质量分数为1-64%=36%,则可求该混合气体10g中的碳元素的质量;根据质量守恒定律的元素守恒,最后碳元素完全进入碳酸钙,可求碳酸钙的质量.
解答:解:由题意“测得某CO与CO2的混合气体中,氧元素的质量分数为64%”,而碳元素的质量分数为1-64%=36%,则:10g×36%=3.6g;根据质量守恒定律的元素守恒,最后碳元素完全进入碳酸钙,则生成碳酸钙的质量是3.6g÷
=30g.
故填:30g.
| 12 |
| 100 |
故填:30g.
点评:本题是运用化学中的基本思想质量守恒思想,通过归纳不同物质或不同变化过程中相同点和不同点有效地寻找出它们之间的内在联系以及融合点和嫁接点,从而培养了学生的创新思维能力.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案
相关题目
如图所示试管的试管口朝向不同可完成不同实验,下列说法错误的是( )
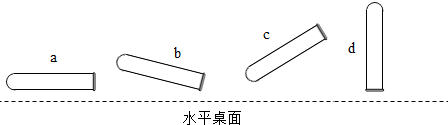

| A、a可用于往试管中添加固体药品 |
| B、b可用于给试管中固体药品加热 |
| C、c可用于给试管中的液体药品加热 |
| D、d可用于排空气法收集少量密度比空气大的气体 |
稀释浓硫酸时,必须把浓硫酸沿着器壁慢慢注入水里,并不断搅动,原因是( )
| A、加快稀释速度 |
| B、浓硫酸具有脱水性 |
| C、浓硫酸具有吸水性 |
| D、浓硫酸溶于水放出大量热并且密度比水大 |
在加油站里应悬挂的警示标志是( )
A、 |
B、 |
C、 |
D、 |
在家用煤气中加入有特殊臭味的乙硫醇可提示煤气是否泄漏.乙硫醇(用X表示)燃烧时发生反应的化学方程式为2X+9O2
4CO2+2SO2+6H2O,则X是( )
| ||
| A、C4H12S2 |
| B、C2H6S |
| C、C2H6O2S |
| D、C2H6 |
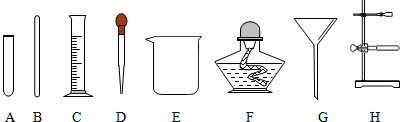
 如图所示A、B、C、D、E都是九年级化学中常见的物质,且相邻物质间均能发生化学反应,A为常见的钾盐,A与B反应有气体生成,B与E反应有白色沉淀生成,C与E为同类物质,B、D均能用于除铁锈.
如图所示A、B、C、D、E都是九年级化学中常见的物质,且相邻物质间均能发生化学反应,A为常见的钾盐,A与B反应有气体生成,B与E反应有白色沉淀生成,C与E为同类物质,B、D均能用于除铁锈.