题目内容
小明在实验室里加热高锰酸钾制取氧气,试管中固体的质量随时间变化的数据见下表.制取结束后,将剩余固体溶解、过滤、烘干后,回收二氧化锰.请计算:
| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 31.6 | 30.2 | 28.4 | 28.4 |
(1)生成氧气的质量为 g.
(2)回收二氧化锰的质量.(写出计算过程)
| 根据化学反应方程式的计算. | |
| 专题: | 综合计算(图像型、表格型、情景型计算题). |
| 分析: | (1)根据质量守恒定律,求出生成氧气的质量; (2)根据生成氧气的质量,利用反应的化学方程式,得出各物质之间的质量比,列出比例式,即可计算出回收二氧化锰的质量. |
| 解答: | 解: (1)根据质量守恒定律,当固体质量变为28.4g时不再减少,故生成氧气的质量为31.6g﹣28.4g=3.2g. (2)设生成MnO2的质量为x 2KMnO4 87 32 X 3.2g
X=8.7g 答案: (1)3.2 (2)回收二氧化锰的质量为8.7g. |
| 点评: | 本题主要考查学生对化学反应方程式的书写,以及运用方程式进行计算的能力. |

 阅读快车系列答案
阅读快车系列答案下列叙述合理且符合质量守恒定律的是( )
|
| A. | 水结成冰前后,质量保持不变 |
|
| B. | 30g过氧化氢溶于70g水中,所得过氧化氢溶液的质量为100g |
|
| C. | 3.2g碳与3.2g氧气完全反应可生成6.4g二氧化碳 |
|
| D. | 3.2g硫与3.2g氧气完全反应可生成6.4g二氧化硫 |
某奶粉包装上的部分文字说明“净含量:300g 钙>400mg 铁:5~10mg”,这里的钙、铁指的是( )
|
| A. | 分子 | B. | 原子 | C. | 离子 | D. | 元素 |
青蒿素(C15H22O5)是我国被世界承认的原创新药.从物质分类看,青蒿素属于( )
|
| A. | 单质 | B. | 氧化物 | C. | 化合物 | D. | 混合物 |
有一硝酸铵样品可能含有下列物质中的一种或几种,经分析,该样品中氮元素的质量分数为20%,那么该样品中一定含有的下列物质是( )
|
| A. | NH4Cl | B. | (NH4)2SO4 | C. | CO(NH2)2 | D. | KNO3 |
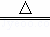 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑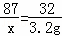 ,
, 2HCl,即想到以下两点,你能想到更多吗?
2HCl,即想到以下两点,你能想到更多吗?