题目内容
14.一定量的硫磺在充满氧气的集气瓶中充分燃烧后,生成了6.4g的二氧化硫气体,则原集气瓶中氧气的质量为( )| A. | 等于3.2g | B. | 小于3.2g | C. | 大于6.4g | D. | 不小于3.2g |
分析 硫在氧气中燃烧生成二氧化硫,由质量守恒定律,反应前后氧元素的质量不变,由生成二氧化硫的质量,计算出参加反应的氧气的质量,进行分析解答即可.
解答 解:硫在氧气中燃烧生成二氧化硫,6.4g的二氧化硫气体中含氧元素的质量为6.4g×$\frac{16×2}{32+16×2}×$100%=3.2g;由质量守恒定律,反应前后氧元素的质量不变,则参加反应的氧气的质量为3.2g,反应后氧气可能有剩余,则原集气瓶中氧气的质量为不小于3.2g.
故选:D.
点评 本题难度不大,理解质量守恒定律、化学式的有关计算并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
5.用燃着的小木条不能鉴别的一组气体是( )
| A. | 空气、氮气、氧气 | B. | 氢气、氧气、二氧化碳 | ||
| C. | 二氧化碳、氮气、空气 | D. | 氧气、二氧化碳、空气 |
2.向AgNO3、Zn(NO3)2的混合溶液中加入过量的铁粉,充分反应后,过滤.则滤出的固体中,一定含有的金属是下列的( )
| A. | 只有Fe和Ag | B. | 只有Zn和Ag | C. | 只有Ag | D. | 只有Fe |
9.下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A. | O | B. | Fe | C. | N2 | D. | Cl- |
11.下列实验操作错误的是( )
| A. |  点燃酒精灯 | B. | 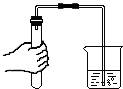 检查装置的气密性 | ||
| C. | 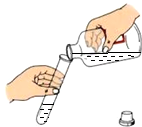 倾倒液体 | D. |  加热液体 |
12.下列关于物质鉴别的方法中错误的是( )
| A. | 水和双氧水可用二氧化锰鉴别 | B. | 汽油和酒精可以通过闻气味鉴别 | ||
| C. | 氮气和空气用带火星的木条鉴别 | D. | 硬水和软水可以用肥皂水鉴别 |