题目内容
17.河南特产“铁棍山药”有很高的营养价值,其主要成分是淀粉、化学式为(C6H10O5)n,下列有关淀粉的说法正确的是( )| A. | 淀粉属于氧化物 | |
| B. | 淀粉中碳、氧两种元素的质量比为9:10 | |
| C. | 淀粉的相对分子质量为162 | |
| D. | 淀粉有碳原子、氢原子和氧原子构成 |
分析 A.根据氧化物的概念来分析;
B.根据淀粉中元素质量比的计算方法来分析;
C.根据相对分子质量的计算方法来分析;
D.根据物质的结构来分析.
解答 解:A.氧化物是由两种元素组成的,而淀粉是由三种元素组成的,不属于氧化物,故错误;
B.淀粉中C、H、O三种元素的质量比为(12×6n):(16×5n)=9:10,故正确;
C.淀粉的相对分子质量为12×6n+1×10+16×5n=162n,故错误;
D.淀粉是由淀粉分子构成的,而不是由原子直接构成的,故错误.
故选B.
点评 本题属于信息习题,学生应能通过信息并结合所学知识来分析,同时通过习题训练学生应注意知识的迁移使用.

练习册系列答案
相关题目
5.某些食品包装袋内常放入还原性铁粉作“双吸剂”以防止食品腐败.某课外兴趣小组在实验室发现了一包破损的还原性铁粉(含少量杂质,杂质既不溶于水也不溶于酸),他们取六份样品,分别加稀硫酸反应.测得部分数据如表,请根据有关信息回答问题.
(1)食品袋内放入“双吸剂”是为了吸收水蒸气和氧气,用铁粉而不用铁块作“双吸剂”的理由是铁粉和水蒸气、氧气接触面积大,反应速率更快、更充分.
(2)a的数值为0.1.
(3)第4次实验,所得到溶液中溶质的化学式为Fe2(SO4)3、FeSO4.
(4)列式计算该样品中单质铁的质量分数(结果精确到0.1%).
| 实验次数 | 1 | 3 | 4 | 5 | 6 |
| 取样品质量(g) | 31.0 | 31.0 | 31.0 | 31.0 | 31.0 |
| 取稀硫酸质量(g) | 30.0 | 90.0 | 120.0 | 150.0 | 180.0 |
| 产生气体质量(g) | 0 | a | 0.3 | 0.5 | 0.6 |
(2)a的数值为0.1.
(3)第4次实验,所得到溶液中溶质的化学式为Fe2(SO4)3、FeSO4.
(4)列式计算该样品中单质铁的质量分数(结果精确到0.1%).
19.下列用化学知识解释的事例正确的是( )
| A. | 空气中的铁比铝更易锈蚀,是因为铁比铝的金属活动性更强 | |
| B. | 生活中用活性炭净化水,是因为活性炭有杀菌作用 | |
| C. | 煤粉碎后燃烧更彻底,是因为粉碎后降低了煤的着火点 | |
| D. | 石灰水能使酚酞试液变红,是因为溶液里含有OH- |
20.已知MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2X+Cl2↑,则X的化学式为( )
| A. | H2 | B. | O2 | C. | H2O | D. | H2O2 |
 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: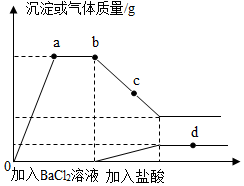 向一定质量的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl
向一定质量的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl