题目内容
18.下列关于分子的叙述中,正确的是( )| A. | 一切物质都是由分子构成 | |
| B. | 分子是不能够再分的粒子 | |
| C. | 分子是保持物质化学性质的最小粒子 | |
| D. | 分子是化学变化中的最小粒子 |
分析 根据已有的分子的性质和分子的知识进行分析解答即可.
解答 解:A、构成物质的基本微粒是分子、原子和离子,错误;
B、分子在化学变化中可以再分,错误;
C、分子是保持物质化学性质的最小粒子,正确;
D、原子是化学变化中的最小粒子,错误;
故选C.
点评 掌握分子的基本性质是正确解答本题的关键.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案
相关题目
8.当前,世界已经迈向了“低碳”时代,选择“低碳”既是一种生活方式也是一种生存责任.孝感市公交系统适应形势发展,推广使用节能减排的双燃料出租车,这种出租车是以天然气为主要燃料.如图为天然气的主要成分甲烷完全燃烧的化学反应的微观示意图.
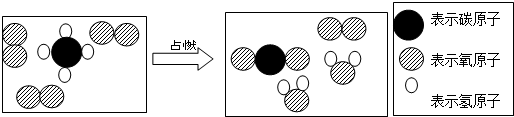
下列说法正确的是( )

下列说法正确的是( )
| A. | 参加反应的两种分子的个数比为1:3 | |
| B. | 使用该燃料,能消除温室效应 | |
| C. | 化学反应前后,碳元素化合价不变 | |
| D. | 原子在化学变化前后种类和个数不变 |
9.某些海鲜中的添加剂“阿斯巴甜”(苯丙氨酸,化学式为C9H11NO2)是一种甜味剂,被苯丙酮尿症患者吸收,将产生严重不良后果.关于苯丙氨酸下列说法不正确的是( )
| A. | 苯丙氨酸属于有机物 | |
| B. | 苯丙氨酸中碳和氧两种元素的质量比是27:8 | |
| C. | 苯丙氨酸中含有1个氮原子 | |
| D. | 苯丙氨酸分子中碳与氢的原子个数比为9:11 |
6.下列实验方案能达到目的是( )
| A. | 测定空气中氧气的体积分数,可以用木炭代替红磷来进行实验 | |
| B. | 比较锌、铁、铜三种金属的活动性顺序,可将光洁的铁丝分别放入硫酸锌和硫酸铜溶液中 | |
| C. | 判断氢氧化钠与稀盐酸反应后溶液的酸碱性,可向反应后的溶液中滴加无色酚酞 | |
| D. | 用带火星的木条鉴别空气、氧气和二氧化碳 |
3.氧气是人类生产生活的重要资源.下列关于氧气的叙述中错误的是( )
| A. | 动植物的呼吸离不开它 | B. | 不易溶于水 | ||
| C. | 具有氧化性,是一种常用的氧化剂 | D. | 能够燃烧 |
18. 已知氯化钠、碳酸钠在不同温度时的溶解度如下:
已知氯化钠、碳酸钠在不同温度时的溶解度如下:
(1)依据上表数据,绘制出了氯化钠和碳酸钠的溶解度曲线(如图),图中能表示碳酸钠溶解度曲线的是A(填“A”或“B”).
(2)图中两溶解度曲线相交于M点,此点表示的意义是30℃时,A和B的溶解度相等.
(3)40℃时,把50g A物质放入100g水中,充分搅拌,所得溶液是溶液饱和(填“饱和”或“不饱和”).
(4)生活在盐湖(主要成分是NaCl和Na2CO3)附近的人们习惯“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”.请你答出“冬天捞碱”的道理碳酸钠的溶解度受温度变化影响较大,温度低时,溶解度较小,温度高时,溶解度较大,冬天温度降低,碳酸钠溶解度较小,会结晶析出.
 已知氯化钠、碳酸钠在不同温度时的溶解度如下:
已知氯化钠、碳酸钠在不同温度时的溶解度如下:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35 | 35.5 | 36 | 36.5 | 37 |
| 碳酸钠 | 6 | 10 | 18 | 36.5 | 50 | |
(2)图中两溶解度曲线相交于M点,此点表示的意义是30℃时,A和B的溶解度相等.
(3)40℃时,把50g A物质放入100g水中,充分搅拌,所得溶液是溶液饱和(填“饱和”或“不饱和”).
(4)生活在盐湖(主要成分是NaCl和Na2CO3)附近的人们习惯“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”.请你答出“冬天捞碱”的道理碳酸钠的溶解度受温度变化影响较大,温度低时,溶解度较小,温度高时,溶解度较大,冬天温度降低,碳酸钠溶解度较小,会结晶析出.