题目内容
1.已知Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO2↑+H2O.一定量Ca(HCO3)2固体在密闭容器中受热分解(此过程CaCO3不分解).下列图象表示此过程中容器内某些量的变化趋势,其中正确的是( )| A. |  | B. | 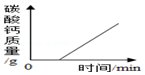 | C. |  | D. | 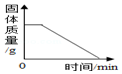 |
分析 根据碳酸氢钙受热分解成碳酸钙、水和二氧化碳,结合反应情况可以判断相关方面的问题.
解答 解:碳酸氢钙在加热的条件下生成碳酸钙、水和二氧化碳,所以
A、依据质量守恒定律可知,碳元素的质量始终不变,故A错误;
B、当碳酸氢钙完全分解后,碳酸钙的质量不再增加,故B错误;
C、加热一段时间后,产生二氧化碳,当碳酸氢钙完全分解后,二氧化碳质量不再增加,故C正确;
D、刚开始加热时,温度不能达到碳酸氢钙的分解温度,因此要经过一段时间后,碳酸氢钙才开始分解,当碳酸氢钙完全分解后,容器中仍然有一定量的固体--碳酸钙,故D错误.
故选:C.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
12.下列化学实验操作顺序正确的是( )
| A. | 氢气还原氧化铜实验中,当氧化铜全部被还原时,先停止通氢气再熄灭酒精灯 | |
| B. | 在精盐提纯实验中,将粗盐溶于水后先加热蒸发再进行过滤 | |
| C. | 加热高锰酸钾制取氧气,用排水法集满氧气后先从水槽中移出导管再熄灭酒精灯 | |
| D. | 用氯酸钾和二氧化锰混合物制取氧气时,先装药品再检验装置的气密性 |
6. 为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
(1)请完成证明金属粉末中存在Fe和Cu的实验设计:
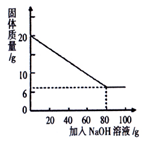
(2)为探究该金属粉末中Al的质量分数,取20g该金属粉末,加入氢氧化钠溶液反应,剩余固体质量与所加氢氧化钠溶液的质量关系如图所示,则该金属粉末中Al的质量分数为70%.
 为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.| 实验操作 | 实验现象 | 结论 |
| I.取少量的金属粉末于试管中,加入足量的氢氧化钠溶液 | 有气泡产生 | 仅除去铝 |
| II.将试管静置,弃去上层清液,加入足量的稀盐酸 | 有气泡产生 | 证明含有铁 |
| III.将试管静置,弃去上层清液,多次洗涤剩余固体 | 剩余固体 呈紫红色 | 证明含有铜 |
(2)为探究该金属粉末中Al的质量分数,取20g该金属粉末,加入氢氧化钠溶液反应,剩余固体质量与所加氢氧化钠溶液的质量关系如图所示,则该金属粉末中Al的质量分数为70%.
13.一瓶未贴标签的粉末状常见金属R.为测定R的相对原子质量,准确称取一定量该金属粉末,在坩埚内加强热使其完全氧化,冷却后再称重.重复实验,获得如表数据.请回答:
(1)表格中m=85.0.
(2)已知R的化合价为+3价,则R的相对原子质量为27.
(3)若用该金属与稀硫酸反应制取0.6克氢气,至少需要质量分数为10%的稀硫酸溶液多少克?
| 实验次数 | 金属质量(g) | 金属氧化物质量(g) |
| l | 45.0 | 84.9 |
| 2 | 45.0 | 85.1 |
| 3 | 45.0 | 85.0 |
| 平均值 | 45.0 | m |
(2)已知R的化合价为+3价,则R的相对原子质量为27.
(3)若用该金属与稀硫酸反应制取0.6克氢气,至少需要质量分数为10%的稀硫酸溶液多少克?
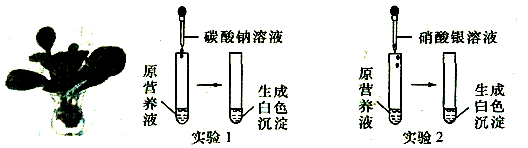
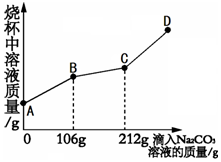 在一烧杯中盛有l00克BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题:
在一烧杯中盛有l00克BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题: