题目内容
7.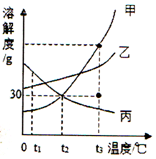 如图是甲、乙、丙三种固体物质的溶解度曲线.根据图中的信息回答下列问题:
如图是甲、乙、丙三种固体物质的溶解度曲线.根据图中的信息回答下列问题:(1)tl℃时,甲的溶解度<乙的溶解度(填“>”、“<”或“二”);
(2)t2°C时,20g丙溶解于50g水中形成65g溶液;
(3)若要将甲的饱和溶液转化为不饱和溶液可采用的一种方法 是升高温度;
(4)t3°C时,将甲、乙、丙三种物质的饱和溶液降温至t2°C,所得溶液溶质质量分数的由大到小的是乙>甲>丙.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)根据图象可以看出,tl℃时,甲的溶解度小于乙的溶解度,故填:<;
(2)t2°C时,丙的溶解度是30g,故20g丙溶解于50g水中,只能溶解15g,故能形成溶液的质量为:15g+50g=65g,故填:65;
(3)甲的溶解度随温度的升高而增大,故要将甲的饱和溶液转化为不饱和溶液可采用升高温度的方法,故填:升高温度;
(4)t3°C时,将甲、乙、丙三种物质的饱和溶液降温至t2°C,甲和乙的溶解度随温度的降低而减小,故会析出晶体变成t2°C时的饱和溶液,在t2°C时乙的溶解度大于甲,故乙的溶质质量分数大于甲的溶质质量分数,而丙的溶解度随温度的降低而增大,溶液的组成不变,根据图象可以看出,丙的溶质质量分数最小,故所得溶液溶质质量分数的由大到小的是乙>甲>丙,故填:乙>甲>丙.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
17.下列图示实验操作中,正确的是(氢氧化钠化学式NaOH,易潮解,强腐蚀)( )
| A. | 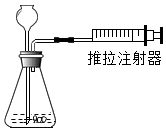 检查装置气密性 | B. |  滴加试剂 | ||
| C. | 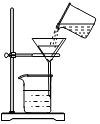 过滤 | D. | 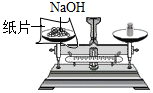 称量氢氧化钠 称量氢氧化钠 |
18.下列实验现象描述不正确的是( )
| A. | 将二氧化碳通入紫色石蕊溶液中,溶液变红 | |
| B. | 铁丝在氧气中剧烈燃烧,火星四射 | |
| C. | 红磷在空气中燃烧,产生大量白烟 | |
| D. | 硫在氧气中燃烧,火焰呈淡蓝色 |
15.向饱和氢氧化钙溶液中加入少量氧化钙固体,充分反应后恢复到原温度,则下列说法正确的是( )
| A. | 反应后溶液质量变大 | B. | 反应后溶剂质量不变 | ||
| C. | 反应后溶质质量变大 | D. | 反应后溶质质量分数不变 |
16.在化学反应A+B═C+D 中,6克A 与8克B 恰好完全反应,生成9克D.则生成C 的质量为( )
| A. | 6克 | B. | 8克 | C. | 5克 | D. | 9克 |
4.某氮的氧化物中,氮、氧元素质量比为7:4,则氧化物的化学式为( )
| A. | NO | B. | N2O | C. | N2O3 | D. | NO2 |
 中国制造业正在持续发展,汽车制造是制造业的一个代表.请根据所学知识按要求填空.
中国制造业正在持续发展,汽车制造是制造业的一个代表.请根据所学知识按要求填空.