题目内容
6.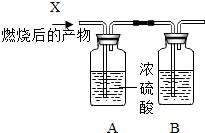 (1)有一瓶纯净气体X,可能是H2、CH4、CO中的一种.现将该气体燃烧后的产物通入如图所示的装置A、B中进行验证.(浓硫酸具有吸水性,可做某些气体的干燥剂).
(1)有一瓶纯净气体X,可能是H2、CH4、CO中的一种.现将该气体燃烧后的产物通入如图所示的装置A、B中进行验证.(浓硫酸具有吸水性,可做某些气体的干燥剂).①是H2,②是CO,③是CH4.
(2)若X可以是其中一种或几种气体的混合物,则:
③是CH4或H2和CO或H2、CO、CH4或H2和CH4或CO、CH4.
| 质量变化 | X | |
| A | B | |
| 增重 | 不变 | ① |
| 不变 | 增重 | ② |
| 增重 | 增重 | ③ |
分析 根据CH4燃烧生成二氧化碳和水;H2燃烧生成水;CO燃烧生成二氧化碳.浓硫酸可吸收水分,质量增加;氢氧化钙溶液可以吸收二氧化碳,质量增加进行分析.
解答 解:(1)①装置A的质量增加,B装置的质量不变,说明有水生成,没有二氧化碳气体生成,则气体是氢气;
②若A装置的质量不变,B装置的质量增加,说明有二氧化碳生成,没有水生成,则气体为一氧化碳;
③若A装置和B装置的质量都增加,说明既有二氧化碳生成,也有水生成,则纯净气体是甲烷.
故答案为:①H2;②CO;③CH4;
(2)A装置和B装置的质量都增加,说明既有二氧化碳生成,也有水生成,则气体中含有氢元素和碳元素的组合即可,因此可以是CH4或H2和CO或H2、CO、CH4或H2和CH4或CO、CH4;
故答案为:CH4或H2和CO或H2、CO、CH4或H2和CH4或CO、CH4.
点评 本题主要考查常见气体燃烧的产物以及根据产物判断物质,要求同学们一定要了解常见物质的性质并熟练运用质量守恒定律.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
17.实验室中有一瓶烧碱固体,打开瓶盖在空气中一段时间后,小王认为它可能变质,请你和他一起探究.
(1)小王认为烧碱暴露在空气中会变质的原因是:2NaOH+CO2═Na2CO3+H2O(写化学方程式),所以保存氢氧化钠必须密封.
(2)小王认为这瓶烧碱的可能组成有:A、全部是烧碱;B、全部是碳酸钠;小李认为还有第三种可能性,请你说出是烧碱和碳酸钠.
(3)对于第三种可能性,小李设计了一下的探究实验,请你帮他一起完成:
(4)请你写出上面第二步的化学方程式:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
(5)步骤3的判断是不正确(填“正确”或“不正确”),理由是因为氢氧化钙溶液显碱性,过量的氢氧化钙溶液能使酚酞试液变红色;再有氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,氢氧化钠能使酚酞试液变红色.
(1)小王认为烧碱暴露在空气中会变质的原因是:2NaOH+CO2═Na2CO3+H2O(写化学方程式),所以保存氢氧化钠必须密封.
(2)小王认为这瓶烧碱的可能组成有:A、全部是烧碱;B、全部是碳酸钠;小李认为还有第三种可能性,请你说出是烧碱和碳酸钠.
(3)对于第三种可能性,小李设计了一下的探究实验,请你帮他一起完成:
| 实验步骤 | 现象 | 结论 |
| 1、取少量固体,往其中滴加稀盐酸. | 有气泡冒出 | 固体中含有碳酸钠 |
| 2、另取少量固体,加水充分溶解,加入过量的氢氧化钙溶液. | 产生白色沉淀 | 固体中含有碳酸钠. |
| 3、对上述反应后的混合物过滤,在滤液中加入酚酞溶液. | 变红色 | 固体中含有氢氧化钠. |
(5)步骤3的判断是不正确(填“正确”或“不正确”),理由是因为氢氧化钙溶液显碱性,过量的氢氧化钙溶液能使酚酞试液变红色;再有氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,氢氧化钠能使酚酞试液变红色.
18.下列物质属于混合物的是( )
| A. | 干冰 | B. | 空气 | C. | 铁 | D. | 五氧化二磷 |
15.下列关于碳和碳的氧化物的说法正确的是( )
| A. | 金刚石、C60和石墨都是由碳原子构成 | |
| B. | CO和CO2都能与碱溶液反应 | |
| C. | CO2与碳的反应时,体现了CO2的氧化性 | |
| D. | CO有还原性,常温下可以将氧化铜中的铜还原出来 |
16.下列物质按单质、碱、混合物的顺序排列的是( )
| A. | 氧气、纯碱、大理石 | B. | 氢气、生石灰、海水 | ||
| C. | 生铁、熟石灰、碘盐 | D. | 水银、苛性钠、石油 |