题目内容
7.如图是实验探究氢气与氧气混合点燃发生爆炸的条件: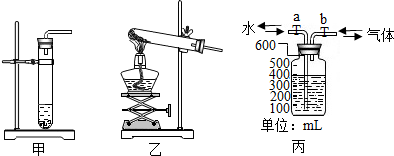
(1)乙装置中对试管加热的仪器名称是酒精灯;在实验室中利用氯酸钾和二氧化锰制取氧气,发生的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;利用锌粒和稀硫酸制取氢气,可以利用下列甲(选填“甲”或“乙”)作为发生装置.写出锌粒与硫酸的化学反应方程式Zn+H2SO4═ZnSO4+H2↑.
(2)利用丙装置可将氢气、氧气收集并混合起来.某次实验的操作过程如下:先将瓶子装满水,打开a、b,从右边导管通入氢气至水面降至400mL,水从左边导管流出(如图),然后继续从右边导管通入氧气至液面降到100mL,关闭b.此时瓶中收集到的混合气体中氢气与氧气的体积比为2:3.打开b,再从左边导管向瓶中加水,使混合气体全部排出,并用一次性保鲜袋收集,直接点燃保鲜袋内的混合气体.实验共四次,实验数据及现象记录如下表,请将表中漏填的数据及现象补填上.
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 氢气与氧气的体积比 | 1:4 | 2:3 | 2:1 | 4:1 |
| 氢气的体积百分数 | 20% | 40% | 66.7% | 80% |
| 点燃后现象 | 爆炸 | 爆炸 | 爆炸 | 保鲜袋燃烧,没有爆炸 |
分析 (1)根据常见仪器的名称,方程式的书写方法考虑,反应物为固体和液体不需要加热;(2)根据水面下降的体积就是收集的气体的体积,根据点燃可燃性气体与空气的混合物容易爆炸,在爆炸极限之内发生爆炸.
解答 解:乙装置中对试管加热的仪器名称是酒精灯;反应物是氯酸钾,生成物是氯化钾和氧气,用观察法配平,氧气后面标上上升符号,所以方程式是:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,锌粒和稀硫酸制取氢气的反应物是固体和液体,不需要加热,发生装置选A;锌与硫酸反应生成硫酸锌和氢气,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
(2)通入氢气至水面降至400mL,所以氢气体积为:600mL-400mL=200mL;继续从右边导管通入氧气至液面降到100mL,所以氧气体积为:400mL-100mL=300mL;混合气体中氢气与氧气的体积比为:200mL:300mL=2:3;
氢气的体积分数是:$\frac{2}{3}$×100%=66.7%;根据第一次和第三次现象可知第二次现象是爆炸.
故答案为:(1)酒精灯;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑; 甲;Zn+H2SO4═ZnSO4+H2↑;
(2)2:3;66.7%;爆炸.
点评 解答本题关键是要熟悉常见仪器的名称,点燃可燃性气体与空气的混合物容易发生爆炸,熟悉方程式的书写方法

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.规范的实验操作是进行科学探究的重要保障,下列实验操作不规范科学的是( )
| A. | 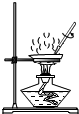 蒸发结晶 | B. | 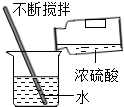 稀释浓硫酸 | C. | 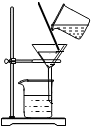 过滤 | D. |  铁丝在氧气中燃 |
19.甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图(未配平)如图所示,根据微观示意图得出的下列结论不正确的是( )
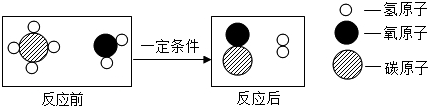

| A. | 反应前后各元素的化合价均不变 | |
| B. | 该反应中含氢元素的化合物有2种 | |
| C. | 该反应为置换反应 | |
| D. | 该反应的化学方程式中甲烷和水的计量数之比为1:1 |
17.下列说法不符合事实的是( )
| A. | 目前使用量最大的金属元素是铝 | |
| B. | 在钢铁表面镀铬能防止钢铁生锈 | |
| C. | 多数合金的抗腐蚀性能比组成它们的纯金属更好 | |
| D. | “真金不怕火炼”说明金的化学性质不活泼 |
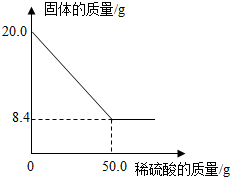 菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示
菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示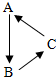 A、B、C均含有质子数为20的元素,它们的转化关系如图(部分物质和反应条件已略去).若B属于氧化物,则A转化为B的化学方程式是CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;由B转化为C的化学方程式为CaO+H2O=Ca(OH)2,该反应过程中的只要现象是固体溶解,放出热量.
A、B、C均含有质子数为20的元素,它们的转化关系如图(部分物质和反应条件已略去).若B属于氧化物,则A转化为B的化学方程式是CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;由B转化为C的化学方程式为CaO+H2O=Ca(OH)2,该反应过程中的只要现象是固体溶解,放出热量.