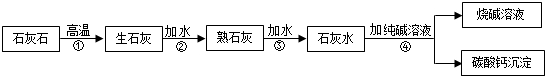
��Ŀ����
12���°桶��������ˮ����������ˮ�ʼ��ָ���ԭ����35�����ӵ�106��Թ�ˮ�����ڵ�ˮ���������Ӧ��Ҫ����1���¹���������ָ���������ӡ�Ǧ�ȵ�������������ӡ�Ǧָ����C������ţ���
A��ԭ�� B������ C��Ԫ�� D������
��2���¹����ж�ˮ��pH�Ĺ涨Ϊ6.5��pH��8.5��ʵ������pH��ֽ�������ˮ��pH=8��˵��������ˮ�Լ��ᡱ��������С����ԣ�
��3���¹�������������1������4������˶��ó������������Ⱥ��Ȱ������Ĺ涨���ٳ�����O3��������������ת��Ϊ����������ת��Ϊ�������ڻ�ѧ������������ߡ���ѧ�����仯���ڶ����������������в����Ĵ���������ӣ�ClO-��Ҳ���������ã�ClO-����Ԫ�صĻ��ϼ�Ϊ+1�ۢ��Ȱ���NH2Cl����3�������֣���Ԫ����ɣ����Ȱ�����ʱ����Ӧ�Ļ�ѧ����ʽ��NH2Cl+X=NH3+HClO������X�Ļ�ѧʽΪH2O��
���� ��1��������������Ԫ����ɵĽ��
��2��������Һ����������ԵĹ�ϵ�������
��3���ٸ��ݱ仯���������
�ڸ��ݻ��ϼ�ԭ�����Ԫ�صĻ��ϼ۽��
�۸��ݻ�ѧʽ��������������������غ㶨�ɿ�֪����Ӧǰ��Ԫ������䣬ԭ�Ӹ������䣬���������ݿ��Ƴ�X�Ļ�ѧʽ��
��� �⣺��1����������Ԫ����ɣ�������ӡ�Ǧָ����Ԫ�أ�
��2���������֪��ʵ������pH��ֽ�������ˮ��pH=8��˵��������ˮ�Լ��ԣ�
��3���������ͳ������ڲ�ͬ�����ʣ���������ת��Ϊ�������ڻ�ѧ�仯��
������Ԫ�صĻ��ϼ�Ϊx
x+��-2��=-1
x=+1
��NH2Cl���е����⡢��3��Ԫ�أ�
����������ѧ����ʽ���Կ�������ѧ����ʽ���ұ߱���߶����2����ԭ�Ӻ�1����ԭ�ӣ����������غ㶨���е�Ԫ��������ԭ�Ӹ���������ص㣬��֪�����ԭ��ȫ������1��X�����У���X�Ļ�ѧʽΪH2O��
�𰸣���1��C����2�����3���ٻ�ѧ����+1����3��H2O��
���� ������Ҫ������������غ㶨���ƶ����ʵĻ�ѧʽ�������ʵĻ�ѧʽ����Ԫ�صĻ��ϼۣ��ѶȽ�С��

��ϰ��ϵ�д�
�����Ŀ
2��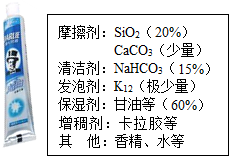 �������������Ʒ��ij��ȤС��ͬѧ��ijƷ���������ࣨ����ͼ��չ������̽������ش����⣺
�������������Ʒ��ij��ȤС��ͬѧ��ijƷ���������ࣨ����ͼ��չ������̽������ش����⣺
�����Ͽ�Ƭ����
a��SiO2������ˮ���Ҳ����ᷴӦ�����²��ֽ⣻
b�������б�ʪ�������������㾫�Ⱦ�Ϊ�л�����º����ӷ�
��1��ȡһС�����࣬��������ˮ����ֽ�����ã�������ϲ���Һ��pHΪ8.3����������Լ��ԣ�ʵ�����ܷ���pH��ֽ��ø���ֵ�����������жϲ�˵�����ɲ��ܣ���Ϊ����pH��ֽ�ⶨ��������������
��2��С��ͬѧ���֣���Ʒ�������ڶ�������ֿ�����������������ʾ�������е�K12��һ�����Σ���������K12���ܽ�Ⱥ��¶ȵĹ�ϵ���ܽ�������¶����߶�����
��3��Ϊ�ⶨ��������SiO2��������������ȤС��ͬѧ��Ʒ�������������3��ʵ�飺
��ʵ�鲽�衿��
��ȷ��ȡ2.0g������壬���ˮ�֣����¼��ȣ����������ټ���Ϊֹ���ڸ���������ȴ�����£�
��ת��ʣ�������ձ��У�����ϡHCl����������ų�
�۹��ˡ�ϴ�ӡ������õ�ʣ������������������
�ܸ���ʵ�����ݽ��м��㣮
�����ݴ�������
��4���˲ⶨ��3��ʵ���Ŀ����ȡƽ��ֵ��ʹ��������ȷ��
��5���ۺ�����ʵ�鷽����ʵ�����ݣ������������SiO2������������22%��
��ʵ���������
��6��������ʵ�鲽����������ֲⶨ���ƫ����ƫ���ԭ�������ʣ���������û�м�ȥ���ݼ���������
��7�����¼��ȵ�Ŀ�ij�Ϊ�˳�ȥCaCO3��NaHCO3���⣬��Ϊ�˳�ȥ��ʪ�������������㾫���л��
��8��������У���ϡHCl�����ķ�Ӧ��CaO+2HCl=CaCl2+H2O��Na2CO3+2HCl=2NaCl+H2O+CO2����
��9��������У�ϴ�ӵ�Ŀ���dz�ȥ���������ϵĸ��������ϴ�ӣ���ⶨ�����ƫ���ƫ����ƫС�����䡱��
��10��Ϊ��֤ϴ��Ч���������Aϴ�ӣ�
A������ˮ B������ˮ C������NaCl��Һ D������CaCl2��Һ��
 �������������Ʒ��ij��ȤС��ͬѧ��ijƷ���������ࣨ����ͼ��չ������̽������ش����⣺
�������������Ʒ��ij��ȤС��ͬѧ��ijƷ���������ࣨ����ͼ��չ������̽������ش����⣺�����Ͽ�Ƭ����
a��SiO2������ˮ���Ҳ����ᷴӦ�����²��ֽ⣻
b�������б�ʪ�������������㾫�Ⱦ�Ϊ�л�����º����ӷ�
��1��ȡһС�����࣬��������ˮ����ֽ�����ã�������ϲ���Һ��pHΪ8.3����������Լ��ԣ�ʵ�����ܷ���pH��ֽ��ø���ֵ�����������жϲ�˵�����ɲ��ܣ���Ϊ����pH��ֽ�ⶨ��������������
��2��С��ͬѧ���֣���Ʒ�������ڶ�������ֿ�����������������ʾ�������е�K12��һ�����Σ���������K12���ܽ�Ⱥ��¶ȵĹ�ϵ���ܽ�������¶����߶�����
��3��Ϊ�ⶨ��������SiO2��������������ȤС��ͬѧ��Ʒ�������������3��ʵ�飺
��ʵ�鲽�衿��
��ȷ��ȡ2.0g������壬���ˮ�֣����¼��ȣ����������ټ���Ϊֹ���ڸ���������ȴ�����£�
��ת��ʣ�������ձ��У�����ϡHCl����������ų�
�۹��ˡ�ϴ�ӡ������õ�ʣ������������������
�ܸ���ʵ�����ݽ��м��㣮
| ʵ���� | 1 | 2 | 3 |
| ʵ��ǰ��g�� | 2.00 | 2.00 | 2.00 |
| ʵ���g�� | 0.43 | 0.44 | 0.45 |
��4���˲ⶨ��3��ʵ���Ŀ����ȡƽ��ֵ��ʹ��������ȷ��
��5���ۺ�����ʵ�鷽����ʵ�����ݣ������������SiO2������������22%��
��ʵ���������
��6��������ʵ�鲽����������ֲⶨ���ƫ����ƫ���ԭ�������ʣ���������û�м�ȥ���ݼ���������
��7�����¼��ȵ�Ŀ�ij�Ϊ�˳�ȥCaCO3��NaHCO3���⣬��Ϊ�˳�ȥ��ʪ�������������㾫���л��
��8��������У���ϡHCl�����ķ�Ӧ��CaO+2HCl=CaCl2+H2O��Na2CO3+2HCl=2NaCl+H2O+CO2����
��9��������У�ϴ�ӵ�Ŀ���dz�ȥ���������ϵĸ��������ϴ�ӣ���ⶨ�����ƫ���ƫ����ƫС�����䡱��
��10��Ϊ��֤ϴ��Ч���������Aϴ�ӣ�
A������ˮ B������ˮ C������NaCl��Һ D������CaCl2��Һ��
3�����жԡ���ѧ���������ʶ������ȷ���ǣ�������
| A�� |  | B�� |  | ||
| C�� |  | D�� |  |
20�������е��������������Լ�ǣ�������
| A�� | 78% | B�� | 21% | C�� | 0.94% | D�� | 0.03% |
17�����������У������л��ϳɲ��ϵ��ǣ�������
| A�� | ���� | B�� | �մ� | C�� | ��ë | D�� | �� |
1��20��ʱ������������a��b���ֹ��壬�ֱ���뵽ʢ��l00gˮ���ձ��У���ֽ����������ͼ�ף����µ�50��ʱ��������ͼ�ң�a��b���ֹ�����ܽ��������ͼ��������˵����ȷ���ǣ�������
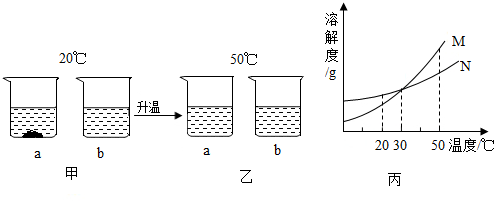

| A�� | ͼ����Һ�����ʵ���������a����b | |
| B�� | ͼ����M��ʾb���ܽ������ | |
| C�� | ͼ����a��Һһ���Dz�������Һ | |
| D�� | 50��ʱa��b������Һ���µ�20��ʱ�������ľ�������a��b�� |
2���Ĵ����ǿ�ѧ�ҷ����˴����²��ϡ�̼������ĭ����ÿ����ĭ����Լ4000��̼ԭ�ӣ��ڵ���-183��ʱ����ĭ�������ô��ԣ����й��ڡ�̼������ĭ��������ȷ���ǣ�������
| A�� | ���ǻ���� | B�� | ���ͽ��ʯ��������ȫ��ͬ | ||
| C�� | ����̼���� | D�� | ����һ�����͵��л��ϳɲ��� |