��Ŀ����
1����ѧʵ���ǽ��п�ѧ̽������Ҫ��ʽ����1������ͼ�ش����⣮
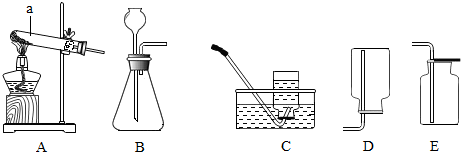
��װ���бꡰa���������������Թܣ�
��ʵ�����Ʊ����ռ�������̼ѡ�õ�װ��ΪBE������ţ���
��ʵ�����ø��������ȡ�����Ļ�ѧ����ʽΪ2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2����
��2����ͼװ�ÿ���һ����̼��ԭ��������ʵ�飬���������ɵ�������

��Bװ�ò�������ɹ۲쵽�������Ǻ�ɫ������ɫ����Ӧ�Ļ�ѧ����ʽΪ��3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��Cװ���з�Ӧ�Ļ�ѧ����ʽΪCa��OH��2+CO2=CaCO3��+H2O��
��3��ijͬѧ��̽���кͷ�Ӧʵ��ʱ������·�����������ϡ���ᵹ����ƿ�У������̪��Һ�������μ�����������Һ�����Ͻ��裬ͨ����Һ�ոձ�����ж��кͷ�Ӧǡ����ɣ���������������Ƿ������˵�����ɣ�
��4����һ��������NaHCO3��Һ��100gϡ�����ϣ�����ǡ����ȫ��Ӧ����Һ������������8.8g����ϡ���������ʵ�����������
���� ��1����dz���������������;��ʵ����ͨ���ô���ʯ��ʯ��ʯ��ϡ���ᷴӦ��ȡ������̼����Ӧ����Ҫ���ȣ�������̼�ܹ�����ˮ���ܶȱȿ��������������ʱ�ܹ��ֽ���������ء��������̺�������
��2���ٸ�����������һ����̼�ڸ��µ��������������Ͷ�����̼���з�����
�ڸ��ݶ�����̼���������Ʒ�Ӧ����̼��Ƴ�����ˮ���з�����
��3�����ݷ�̪��Һ������������Һ�����
��4������̼�����ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼�����ݶ�����̼���������м��㣮
��� �⣺��1����a���Թܣ�����ʵ�����У���ȡ������̼����Ҫ���ȣ�Ӧ����Bװ����Ϊ����װ�ã�������̼�ܹ�����ˮ����������ˮ���ռ����ܶȱȿ��������������ſ������ռ�������Eװ���ռ������B��E��
�۸����������ʱ�ܹ��ֽ���������ء��������̺�����������ʽΪ��2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2����
��3������������һ����̼�ڸ��µ��������������Ͷ�����̼������Bװ�ò�������ɹ۲쵽������Ϊ����ɫ�����ڣ���ѧ����ʽΪ��3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
�ڶ�����̼���������Ʒ�Ӧ����̼��Ƴ�����ˮ����ѧ����ʽΪ��CO2+Ca��OH��2=CaCO3��+H2O��
��3��������ϡ���ᵹ����ƿ�У������̪��Һ�������μ�����������Һ�����Ͻ��裮ǡ����ȫ�к�ʱ��Һ����ɫ����Һ�ոձ�죬˵�����������Ѿ�������
��4����μӷ�Ӧ�����������Ϊx
NaHCO3+HCl=NaCl+H2O+CO2��
36.5 44
x 8.8g
$\frac{36.5}{x}=\frac{44}{8.8g}$
x=7.3g
����ϡ���������ʵ���������Ϊ��$\frac{7.3g}{100g}$��100%=7.3%��
�ʴ�Ϊ����1�����Թܣ���B E�� ��2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2����
��2���ٺ�ɫ������ɫ��3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��Ca��OH��2+CO2=CaCO3��+H2O��
��3����������ǡ����ȫ�к�ʱ��Һ����ɫ��
��4��7.3%��
���� �����ۺϿ�����������Ʊ���һ����̼��ԭ���������кͷ�Ӧ���ж��Լ���ѧ����ʽ�ļ��㣬�ѶȲ�������㣮

| A�� | �������� | B�� | ţ�̱��� | C�� | �����ۻ� | D�� | �ƾ��ӷ� |
| A�� | �����谷����3��̼ԭ�ӡ�6����ԭ�ӡ�6����ԭ����� | |
| B�� | �����谷����Է�������Ϊ126 | |
| C�� | �����谷��̼���⡢��Ԫ�ص�������Ϊ6��1��14 | |
| D�� | �����谷�е�Ԫ����������Ϊ66.7% |
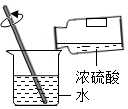 ϡ��Ũ����
ϡ��Ũ����

 ����NaOH����
����NaOH����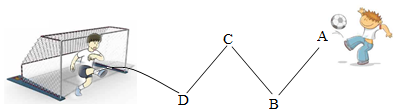 ������������һ��������Ϸ����Ϸ�����ǣ�����Ա��֮�������Ӧ����Ч��������Ա���롰��Ա��֮���ܷ�Ӧ�����ųɹ���������ӡ�������ϡ���ᡢ�������ơ�����ͭ��������Ա����ɣ���Ϸ�У��ɡ�A��Ա������ͭ������·�ߺ�������ͼ��ʾ��������Ա���Ǹ�������֡���
������������һ��������Ϸ����Ϸ�����ǣ�����Ա��֮�������Ӧ����Ч��������Ա���롰��Ա��֮���ܷ�Ӧ�����ųɹ���������ӡ�������ϡ���ᡢ�������ơ�����ͭ��������Ա����ɣ���Ϸ�У��ɡ�A��Ա������ͭ������·�ߺ�������ͼ��ʾ��������Ա���Ǹ�������֡���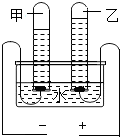 ˮ�����������ϢϢ��أ�
ˮ�����������ϢϢ��أ� С��ѧϰ�˵��ʡ�������ᡢ������ʺ������ͬ�������ʷ�Ӧʱ���������Σ���������������ͼ��ʾ��֪ʶ����ͼ����ϴ�ͼ�ش��������⣺
С��ѧϰ�˵��ʡ�������ᡢ������ʺ������ͬ�������ʷ�Ӧʱ���������Σ���������������ͼ��ʾ��֪ʶ����ͼ����ϴ�ͼ�ش��������⣺