题目内容
小皓同学在做实验时,将21g碳酸镁粉末加入一定量的稀硫酸中,恰好完全反应得到澄清溶液,其反应的化学方程式为:MgCO3+H2SO4═MgSO4+H2O+CO2↑,反应后所得溶液中溶质质量分数为20%.请计算:
(1)小皓将反应后的溶液蒸干可以得到固体多少克?
(2)小皓所用的稀硫酸中溶质的质量分数是多少?
(1)小皓将反应后的溶液蒸干可以得到固体多少克?
(2)小皓所用的稀硫酸中溶质的质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)依据碳酸镁的质量利用方程式即可计算生成的硫酸镁的质量;
(2)利用硫酸镁的质量和所得溶液的溶质质量分数即可求出反应后溶液的质量,进而可得硫酸溶液的质量,而后利用硫酸的质量即可计算硫酸的溶质质量分数;
(2)利用硫酸镁的质量和所得溶液的溶质质量分数即可求出反应后溶液的质量,进而可得硫酸溶液的质量,而后利用硫酸的质量即可计算硫酸的溶质质量分数;
解答:解:(1)设反应生成的硫酸镁的质量是x,反应的硫酸的质量是y,生成的水的质量是z
MgCO3+H2SO4═MgSO4+H2O+CO2↑
84 98 120 18
21g y x z
=
=
=
x=30g y=24.5g z=4.5g
(2)反应后所得溶液的质量是
=150g,故稀硫酸中水的质量为150g-30g-4.5g=115.5g,故硫酸溶液的溶质质量分数为
×100%=17.5%
答:(1)小皓将反应后的溶液蒸干可以得到固体30g;
(2)小皓所用的稀硫酸中溶质的质量分数是17.5%.
MgCO3+H2SO4═MgSO4+H2O+CO2↑
84 98 120 18
21g y x z
| 84 |
| 21g |
| 98 |
| y |
| 120 |
| x |
| 18 |
| z |
x=30g y=24.5g z=4.5g
(2)反应后所得溶液的质量是
| 30g |
| 20% |
| 24.5g |
| 115.5g+24.5g |
答:(1)小皓将反应后的溶液蒸干可以得到固体30g;
(2)小皓所用的稀硫酸中溶质的质量分数是17.5%.
点评:此题是依据化学方程式计算的考查题,解题的关键是能够掌握有关计算时的待求量.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目

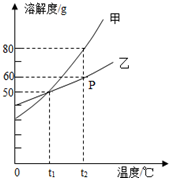 如图是甲、乙两种固体物质的溶解度曲线,请回答下列问题.
如图是甲、乙两种固体物质的溶解度曲线,请回答下列问题.