题目内容
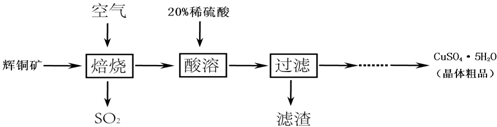
18.硫酸铜溶液常用于农业上制波尔多液.如图是用废铜料(铁、铜混合物)来生产硫酸铜的过程,请根据图示回答下列问题.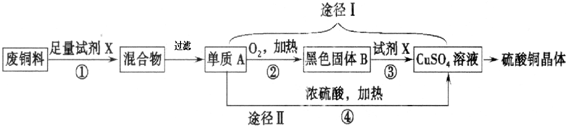
(1)反应①的基本类型为置换反应;
(2)③反应的化学方程式为CuO+H2SO4═CuSO4+H2O;
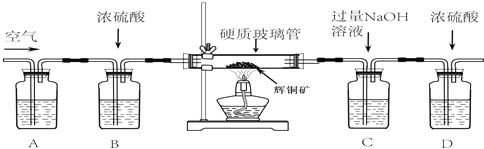
(3)已知:Cu+2H2SO4 (浓)$\frac{\underline{\;加热\;}}{\;}$ CuSO4+SO2↑+2M.则M的化学式为H2O;对比途径I、Ⅱ,途径I的优点有:不产生污染环境的二氧化硫.
分析 铁能和稀硫酸反应生成硫酸亚铁和氢气,铜在加热条件下能和氧气反应生成黑色固体氧化铜,氧化铜和稀硫酸反应生成硫酸铜和水;
化学反应前后,元素的种类不变,原子的种类、总个数不变;
二氧化硫有毒,扩散到空气中会污染环境.
解答 解:铁能和稀硫酸反应生成硫酸亚铁和氢气,铜在加热条件下能和氧气反应生成黑色固体氧化铜,氧化铜和稀硫酸反应生成硫酸铜和水,因此X是稀硫酸,A是铜,B是氧化铜;
(1)反应①中,铁和稀硫酸反应生成硫酸亚铁和氢气,属于置换反应.
故填:置换反应.
(2)③中,氧化铜和稀硫酸反应生成硫酸铜和水,反应的化学方程式为:CuO+H2SO4═CuSO4+H2O.
故填:CuO+H2SO4═CuSO4+H2O.
(3)由Cu+2H2SO4 (浓)$\frac{\underline{\;加热\;}}{\;}$ CuSO4+SO2↑+2M可知,反应前后铜原子都是1个,硫原子都是1个;
反应前氢原子是4个,反应后应该是4个,包含在2M中,反应前氧原子是8个,反应后应该是8个,其中2个包含在2M中,则M的化学式为H2O;
对比途径I、Ⅱ,途径I的优点是不产生污染环境的二氧化硫.
故填:H2O;不产生污染环境的二氧化硫.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
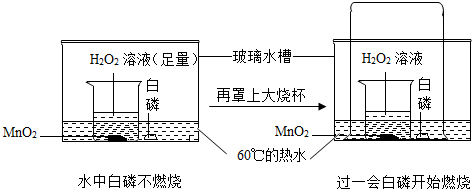
7.有关催化剂的说法正确的是( )
| A. | 催化剂只能加快化学反应速率 | |
| B. | 化学反应前后催化剂的质量不变 | |
| C. | 所有化学反应都需要催化剂 | |
| D. | 化学反应前后催化剂的化学性质改变 |
6.下列有关溶液的叙述错误的是( )
| A. | 溶液是均一、稳定的混合物 | |
| B. | 固体NaOH溶于水时,溶液温度升高 | |
| C. | 一定条件下,饱和溶液和不饱和溶液可以相互转化 | |
| D. | 溶液中的溶剂只能是水 |
7.如下表为NH4Cl、NaCl、KNO3在不同温度下溶解度,根据表中的数据,回答下列问题:
(1)根据NH4Cl和NaCl的溶解度随温度的变化的情况,写出它们具有 相同的溶解度的温度范围(跟相邻两个温度之间)10℃--20℃.
(2)600C时,配制KNO3溶液,质量分数最大的是52.4%.
(3)若KNO3中含有少量NaCl应采取的分离方法是降温结晶法.
 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | 138 | 169 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 |
| NH4Cl | 29.4 | 33.3 | 37.6 | 41.4 | 45.8 | 50.4 | 55.2 | 55.2 | 65.6 |
(2)600C时,配制KNO3溶液,质量分数最大的是52.4%.
(3)若KNO3中含有少量NaCl应采取的分离方法是降温结晶法.