题目内容
载人宇宙飞船内常用含氢氧化锂(LiOH是一种可溶性碱,具有碱的通性)的过滤网吸收宇航员呼出的CO2,以净化空气。若载人宇宙飞船内每名宇航员平均每天呼出的CO2为550升,请回答:
(1)每天吸收一位宇航员呼出的CO2需氢氧化锂多少克?(列式计算,计算时CO2密度以ρ=2.0 g·L-1计)
(2)载人宇宙飞船使用的过滤网内选用氢氧化锂,而不用价格更便宜的氢氧化钠,其主要原因是___________________________________________________
____________________________________________________。
本题考查涉及体积的化学方程式的计算。
(1)根据公式m=ρV,可求得二氧化碳的质量,代入化学方程式可得氢氧化锂的质量。(2)氢氧化钠俗称火碱、烧碱、苛性钠,腐蚀性太强,故不用氢氧化钠(或吸收等质量二氧化碳需要氢氧化锂的质量少,这样可以减小飞船的载重)。
答案:(1)解:设需要消耗氢氧化锂的质量为x
m(CO2)=ρV=2.0 g·L-1×550 L=1 100 g
2LiOH + CO2====Li2CO3+ H2O
48 44
x 1 100 g
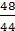 =
=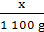 x=1 200 g
x=1 200 g
(2)吸收等质量二氧化碳需要氢氧化锂的质量少,这样可以减小飞船的载重(或氢氧化钠具有强烈腐蚀性)

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目




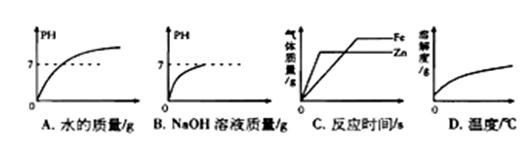

 温度的关系
温度的关系