题目内容
5.通过下列各组对比试验,能够得到相应结论的是( )| A. | 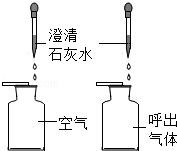 人呼出的气体中CO2含量高于空气 | B. | 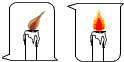 燃烧需要可燃物 | ||
| C. | 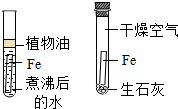 铁生锈需要氧气和水 | D. |  氢离子使石蕊试液变红 |
分析 二氧化碳能使澄清石灰水变浑浊;
燃烧的条件是:有可燃物,可燃物与氧气接触,温度达到着火点;
铁和水、氧气同时接触时容易生锈;
显酸性的溶液能使石蕊试液变红色.
解答 解:A、过程中,滴入呼出气体中的澄清石灰水变浑浊比滴入空气中的澄清石灰水变浑浊明显,因此人呼出的气体中二氧化碳含量高于空气;
B、过程中,倒扣烧杯中的蜡烛熄灭,另一只蜡烛不能熄灭,说明燃烧需要氧气;
C、过程中,铁都不能生锈,说明铁单独和水或氧气接触不能生锈,但是不能说明铁生锈的条件;
D、稀盐酸中含有氢离子、氯离子和水分子,氯化钠溶液中含有钠离子、氯离子和水分子,氯化钠溶液不能使石蕊试液变红色,而稀盐酸能使石蕊试液变红色,说明氢离子能使石蕊试液变红色.
故选:AD.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.20℃时,氯化钠的溶解度为36g.将40克氯化钠放入100克水中,所得氯化钠的饱和溶液的质量是多少( )
| A. | 40g | B. | 140g | C. | 136 g | D. | 100 g |
13.下列物质中,属于盐的是( )
| A. | 氢氧化铝 | B. | 尿素CO(NH2)2 | C. | 氧化钡 | D. | 氯化镁 |
20.用碳化钙等原料制得纯度99%以上的乙炔,乙炔连续热解后得到炭黑,该炭黑称为“乙炔炭黑”.下列关于“乙炔炭黑”的说法错误的是( )
| A. | 常温下化学性质活泼 | B. | 具有吸附性 | ||
| C. | 在一定条件下可还原氧化铜 | D. | 在氧气中完全燃烧的产物是CO2 |
10.硬脂酸的化学式可用RCOOH表示,由硬脂酸和氢氧化钠反应生成的硬脂酸钠作为凝固剂,将酒精和硬质酸钠调匀可得固体酒精.固体酒精在较高的温度下燃烧时,硬质酸钠可先完全转化为硬脂酸和氢氧化钠,硬脂酸和酒精均可完全燃烧生成二氧化碳和水.回答下列问题:
(1)硬脂酸在水中可电离出RCOO-离子和H+.
(2)硬脂酸的组成元素为C、H、O.
(3)写出硬脂酸和氢氧化钠溶液反应的化学方程式RCOOH+NaOH=RCOONa+H2O.
取少量固体酒精置于蒸发皿中,用火柴点燃,固体酒精完全燃烧后,蒸发皿中残余了少量的白色固体.
【发现问题】固体酒精燃烧后留下的白色固体成分是什么呢?
【进行猜想】
猜想I:白色固体是NaOH 猜想II:白色固体是Na2CO3
猜想III:白色固体是NaOH、Na2CO3.
【实验探究】限选试剂:酚酞溶液、蒸馏水、氯化钡溶液、氯化铁溶液、稀盐酸.
(1)硬脂酸在水中可电离出RCOO-离子和H+.
(2)硬脂酸的组成元素为C、H、O.
(3)写出硬脂酸和氢氧化钠溶液反应的化学方程式RCOOH+NaOH=RCOONa+H2O.
取少量固体酒精置于蒸发皿中,用火柴点燃,固体酒精完全燃烧后,蒸发皿中残余了少量的白色固体.
【发现问题】固体酒精燃烧后留下的白色固体成分是什么呢?
【进行猜想】
猜想I:白色固体是NaOH 猜想II:白色固体是Na2CO3
猜想III:白色固体是NaOH、Na2CO3.
【实验探究】限选试剂:酚酞溶液、蒸馏水、氯化钡溶液、氯化铁溶液、稀盐酸.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量该固体于烧杯中,加蒸馏水溶解 | 固体全部溶解,有热量放出 | 固体可能含有NaOH. |
| ②取①所得的溶液于试管中,滴加几滴酚酞溶液 | 溶液显红色 | 猜想III成立 |
| ③取①所得的溶液于试管中,滴加氯化钡溶液. | 出现白色沉淀. |
6.在2010年温哥华冬奥会上,加拿大向世人展示了胆识和理念,他们用从14万吨电子垃圾(废旧显像管、电脑配件、电路板等)中提取出来的金银铜制成精致漂亮的奖牌,下列有关说法中正确的是( )
| A. | 废弃的电子垃圾中只含有金银铜等金属 | |
| B. | 合理回收处理电子垃圾既可以改善环境,又可以节约资源 | |
| C. | 通过焚烧可以清除电子垃圾对环境的污染 | |
| D. | 电子垃圾填埋不会造成地下水资源严重污染 |
4.下列溶液中酒精为溶剂的是( )
| A. | 酒精溶液 | B. | 碘酒 | C. | 酒精的汽油溶液 | D. | 葡萄酒 |
