题目内容
10.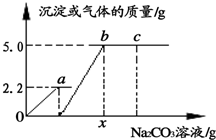 向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.试回答下列问题:
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.试回答下列问题:①oa段表示生成气体(填“气体”或“沉淀”)的质量;
②c点对应的溶液中溶质为Na2CO3、NaCl;
③x值为106.0g.(写出计算过程)
分析 根据加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀,最后到达最高点说明已经反应完了解答.
解答 解:
①加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,故图中oa段表示生成的气体质量;
②加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀,最后到达最高点说明已经反应完了,C点时碳酸钠溶液过量,c点的溶液中含有Na2CO3、NaCl两种溶质;
③根据题意可知碳酸钠先与盐酸反应,再与氯化钙反应,由图示可知碳酸钠与盐酸反应生成气体2.2g,碳酸钠与氯化钙反应,生成沉淀5.0g.设生成2.2g气体所需的Na2CO3的质量为y,生成沉淀5.0g所需Na2CO3的质量为z.则
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
y 2.2g
$\frac{106}{y}=\frac{44}{2.2g}$
解得,y=5.3g;
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
z 5.0g
$\frac{106}{z}=\frac{100}{5.0g}$
解得z=5.3g;
所以x=$\frac{5.3g+5.3g}{10%}$=106.0g;
答案:
①气体
②Na2CO3、NaCl
③106.0g
点评 解答本题关键要知道只有把盐酸反应完了,才能与氯化钙反应产生沉淀,因为如果碳酸钠与氯化钙先反应生成了碳酸钙沉淀,也会被剩余的盐酸溶解掉,将不会看到沉淀.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.按酸、碱、盐、氧化物的顺序排列的一组物质是( )
| A. | H2SO4 NaOH Na2CO3 Fe2O3 | |
| B. | H2O Ca(OH)2 HCl Na2SO4 | |
| C. | H2SO4 Na2CO3 NaCl CuO | |
| D. | NaOH H2CO3 NaCl CO2 |
5.化学上把一种元素组成的不同单质称作同素异形体,下面各组物质是同素异形体的是( )
| A. | 水和过氧化氢 | B. | 氧气和臭氧 | C. | 金刚石和煤炭 | D. | 天然气和甲烷 |
15.2g氢气和2g氧气在点燃条件下充分反应,能生成水( )
| A. | 18 g | B. | 4.5 g | C. | 2.25 g | D. | 36 g |
2.下列不能用质量守恒定律解释的是( )
| A. | 鲜牛奶变质 | B. | 粮食酿成酒 | C. | 钢丝球刷碗 | D. | 煤炭的燃烧 |
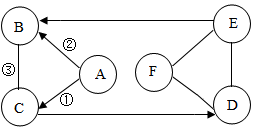 A、B、C、D、E、F都是初中化学常见的物质,A、C都是维系人类生命最重要的物质,B是用于光合作用和灭火的气体,D可用于保护树木,防止冻伤,并防止害虫生卵,E中含有两种元素,它们之间的转化关系如图所示.(“-”表示两端的物质能发生化学反应;“→”表示物质之间的转化关系.)
A、B、C、D、E、F都是初中化学常见的物质,A、C都是维系人类生命最重要的物质,B是用于光合作用和灭火的气体,D可用于保护树木,防止冻伤,并防止害虫生卵,E中含有两种元素,它们之间的转化关系如图所示.(“-”表示两端的物质能发生化学反应;“→”表示物质之间的转化关系.)